Впч вкр 16 лечение
- ВПЧ – Вирус Папилломы Человека
HPV — Human PapillomaVirus
Папилломавирусы — это группа ДНК-содержащих вирусов, поражающих клетки эпителия органов и тканей: кожи, слизистых оболочек.
В чём опасность ВПЧ 16 типа для женщин?
Характерная особенность папилломавирусов — способность индуцировать образование различных эпителиальных опухолей.
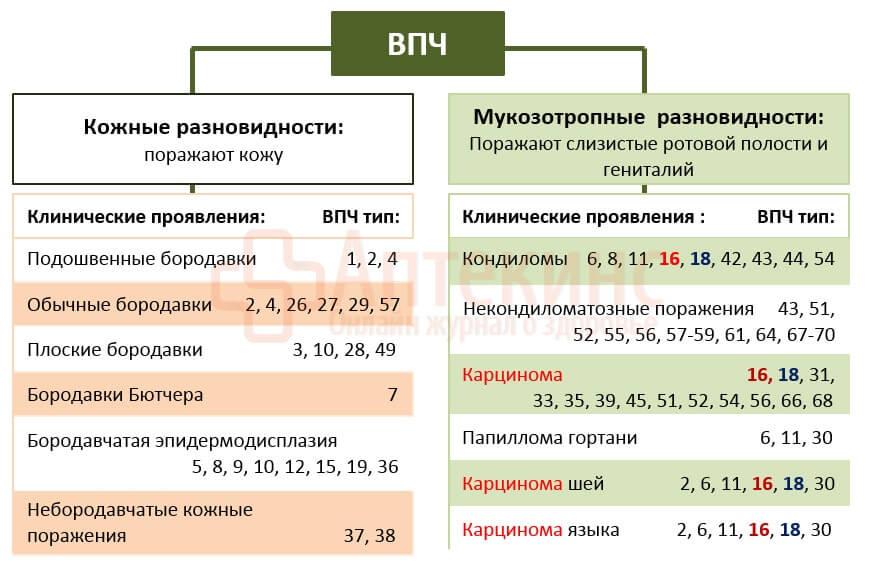
Формы повреждения тканей, вызванных ВПЧ, многообразны. Встречаются бессимптомные и малозаметные: кератозы, дисплазии. Бывают клинически ярко выраженные: бородавки, папилломы, кондиломы. Большинство абсолютно безопасны. Без лечения они остаются пожизненным косметическим дефектом или исчезают самостоятельно (самоизлечение).
Но иногда доброкачественные поражения могут перерождаться в злокачественные опухоли – карциномы.
- Карцинома или эпителиальный рак – это злокачественная опухоль, которая развивается из изменённых клеток эпителия различных тканей.
На сегодняшний день установлено, что папилломавирусная инфекция – ведущая причина развития рака шейки матки. При клинически выраженном цервикальном раке ВПЧ высоких рисков онкогенности выявляется в 95-100% случаях.
Известно около 100 серотипов папилломавирусов. Около 17 считаются онкогенными.
- В группу наиболее высокого риска входят ВПЧ типов: 16, 18, 31, 33, 35, 39, 45, 46, 51, 52, 56, 58, 59 и 68.
- Вирусами низкого риска остаются ВПЧ типов: 6, 11, 42, 43, 44.

Для женщин особенно опасны ВПЧ 16 и 18 типов: они чаще всего вызывают рак шейки матки.

На ВПЧ 16/18 приходится 70% ассоциированного с папилломавирусной инфекцией цервикального рака. Причём наиболее распространённый плоскоклеточный рак связывают с ВПЧ 16 типа. А редко встречающийся железистый рак – с ВПЧ 18 типа.
Заражение ВПЧ 16 типа
Распространённость папилломавирусной инфекции чрезвычайно велика: ДНК тех или иных (иногда сразу нескольких) типов ВПЧ обнаруживаются более чем у 80% взрослого населения.
Мукозотропные ВПЧ, в том числе серотип 16, относят к инфекциям, передающимся половым путём (ИППП). Вероятность заражения через кровь, предметы быта, тем более воздушно-капельным путём ничтожна.
Пути заражения ВПЧ 16 типа:
- Половой путь: традиционный, оральный, нетрадиционный сексуальный контакт с инфицированным партнёром.
- Внутриутробно: заражение плода от инфицированной матери через плаценту или околоплодные воды.
- Во время родов: заражение новорожденного при прохождении по поражённым кондиломами родовым путям матери.
Что происходит после заражения ВПЧ 16 типа?
Подавляющее большинство инфицированных ВПЧ не подозревают о случившемся и в дальнейшем не имеют никаких осложнений.
Более того, до 75% сексуально активных женщин на протяжении жизни заражаются различными типами ВПЧ по нескольку раз. Однако у 2/3 женщин активная инфекция через некоторое время частично или полностью выводится из организма системой иммунитета.
«Остатки» вирусов «консервируются» в чувствительных тканях в виде ДНК ВПЧ и наследуются внутри заражённого клона клеток на протяжении всей жизни носителя. В момент ослабления местного или общего иммунитета скрытая ВПЧ-инфекция «просыпается», рецидивирует, проявляется клинически.
Причины снижения иммунитета к ВПЧ 16 типа у женщин:
— беременность;
— возрастные изменения, связанные со старением организма;
— острые, хронические гинекологические, соматические, воспалительные, инфекционные заболевания;
— ИППП: хламидиоз, генитальный герпес, ЦМВИ, трихомониаз, гонорея, сифилис, ВИЧ, др.
— гормональный дисбаланс;
— нейроэндокринные, метаболические нарушения, ожирение;
— операции, травмы, аборты, тяжёлые роды;
— хронический стресс, физическое истощение;
— лечение цитотоксическими, иммуносупрессивными препаратами;
— агрессивная инсоляция, ионизирующее облучение, лучевая терапия;
— курение, алкоголизм.
Длительное малопродуктивное персистентное течение ВПЧ-инфекции возможно только на фоне дефектов иммунитета.
Симптомы ВПЧ 16 типа у женщин
- Латентная инфекция – симптомов нет.
Присутствие вируса можно выявить лишь с помощью современных иммунохимических или молекулярно-биологических методик, которые определяют наличие в организме антигенов или ДНК ВПЧ.
У женщин даже бессимптомное течение ВПЧ 16 типа может инициировать рак шейки матки.
- Субклиническая
ВПЧ-инфекция персистирует (то обостряется, то стихает), протекает малозаметно, на фоне хронического вульвогинита, эндоцервицита, псевдоэрозии шейки матки. Иногда пациентку беспокоят жжение, зуд в генитальной области. Возможны скудные аномальные выделения из влагалища, дизурические явления.
В цервикальных мазках появляются: койлоциты, лейкоциты, атипичные клетки; иногда — патогенная флора (сочетание ВПЧ-инфекции с другими ИППП вполне закономерно).
Каким должен быть мазок из влагалища у здоровой женщины подробно читайте в статье: Повышенные лейкоциты в мазке у женщины – причины.
В гистологических препаратах цервикальной слизистой видны патологические изменения структуры эпителия шейки матки. При опухолевой трансформации появляется дисплазия (неоплазия, ЦИН).
- Клинически выраженная
ВПЧ-инфекция у женщин – это папилломатоз или кондиломатоз вульвы, влагалища, шейки матки, аногенитальной области.
Как вылечить кондиломы, как выглядят аногенитальные бородавки — читайте подробно в статье: Кондиломы остроконечные.
ВПЧ 16 типа и рак шейки матки

В состав папилломавирусов высокого риска входят специфические структурные белки-онкопротеины Е6 и Е9. Они способны инактивировать внутриклеточный иммунитет. Их особенно много в ВПЧ 16 типа. Вызывая генетическую нестабильность, онкопротеины ВПЧ 16 инициируют мутацию клеток, развитие интраэпителиальной неоплазии, рака шейки матки.
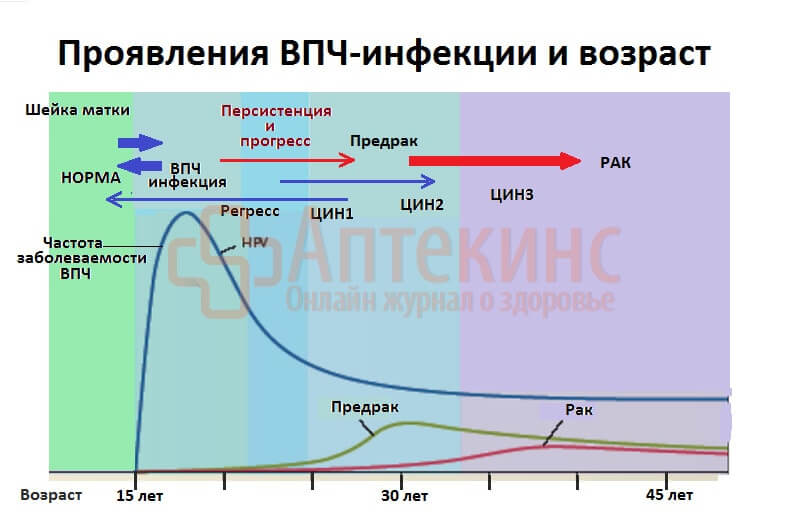
Дисплазия шейки матки или цервикальная интраэпителиальная неоплазия (ЦИН/CIN) – это нарушение структуры эпителиальных пластов цервикальной слизистой. Патологический процесс обусловлен аномальным размножением (пролиферацией) атипичных, трансформированных ВПЧ, клеток.
Цервикальная дисплазия – раннее проявление папилломавирусной инфекции, вызванной ВПЧ 16 и 18 типов.
Умеренная и тяжёлая дисплазия (ЦИН 2-3) – предраковое состояние. Без лечения к 40-49 годам на фоне возрастных изменений иммунитета она может малигнизироваться в клинически выраженный (инвазивный) рак. Злокачественное перерождение прогрессирует очень медленно, годами.
Своевременное выявление и адекватное лечение ЦИН полностью предотвращает развитие рака шейки матки.
Вот почему каждая женщина, ведущая половую жизнь, должна делать плановую скрининг-диагностику ВПЧ и сдавать мазок на онкоцитологию (ПАП-тест).
ДНК-диагностика ВПЧ 16 типа у женщин
Материалом для данного исследования служат: влагалищный мазок или цервикальный соскоб.
Есть два основных молекулярных метода выявления и верификации серотипов ВПЧ:
1. ПЦР — метод полимеразной цепной реакции.
Позволяет найти в исследуемом материале ДНК определённого типа ВПЧ. ПЦР-тест высокочувствителен. Он выявляет даже минимальное количество вирусного генетического материала.
Но!
По его результатам сложно отличить активный инфекционный процесс от безопасного латентного ВПЧ-носительства.
Расшифровка результатов ПЦР-теста на онкогенные ВПЧ 16/18 типов
| HPV 16/18, ДНК ПЦР-тест | Что значит? |
| Отрицательный | В биоматериале не найдено ДНК ВПЧ 16/18 типа: онкогенная ВПЧ-инфекция маловероятна. Повторный скрининг-тест через 2-3 года. |
| Положительный | В биоматериале обнаружены ДНК ВПЧ 16/18 типа. Рекомендовано: ПАП-тест + консультация специалиста. |
2. Метод гибридного захвата или ВПЧ Digene-Тест (НС2)
система двойной генной ловушки.
Преимущество Дайджен-теста перед ПЦР —
количественное определение клинически значимого уровня вирусной нагрузки.
Для выявления концентрации единственных серотипов ВПЧ 16/18 иногда используются ВПЧ-скрининг-тесты АмплиСенс ВПЧ 16/18-FL.
Клинически значимый (референсный) уровень вирусной нагрузки
| ВПЧ-тест | Пороговый уровень ДНК ВПЧ |
| Digene HPV-test | 1 pg/ml (или 105 копий ДНК ВПЧ в 1 мл) |
| ВПЧ тесты АмплиСенс | 3 lg на 105 клеточных геномов |
Расшифровка:
- «ДНК не обнаружено»
или
«-» результат отрицательный (концентрация ДНК ВПЧ меньше пороговой).
В биоматериале не найдено ДНК вируса или вирусная нагрузка клинически незначима.
Рекомендации: профилактическое посещение гинеколога 1 раз в год. Повторить ДНК ВПЧ-тест через 2-3 года.
- Результат «+» положительный:
Вирусная нагрузка превышает допустимый уровень.
Рекомендации: ПАП-тест, консультация специалиста, и, в случае необходимости, дальнейшее обследование.
Цитологическая диагностика ВПЧ 16 типа у женщин
Мазок на цитологию шейки матки = ПАП-тест.
Это исследование окрашенных мазков-отпечатков соскоба поверхности шейки матки под микроскопом.
Расшифровка:
- NILM — морфологически изменённых, атипичных клеток в мазке нет. Это значит, что ВПЧ-инфекции нет или она существует в безопасной латентной форме.
- КА, ASC, SIL — в мазке видны клетки шеечного эпителия, поражённые ВПЧ: койлоциты, дискератоциты (клетки плоского эпителия маленького размера с ороговевшей цитоплазмой), атипичные клетки, что указывает на субклиническое или клиническое течение ВПЧ.
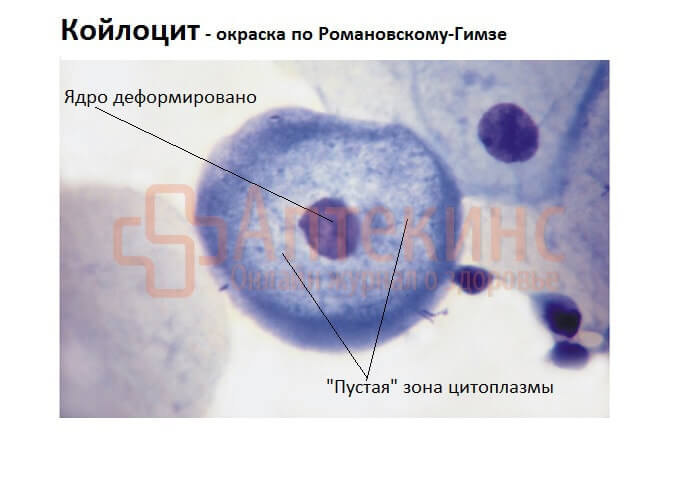
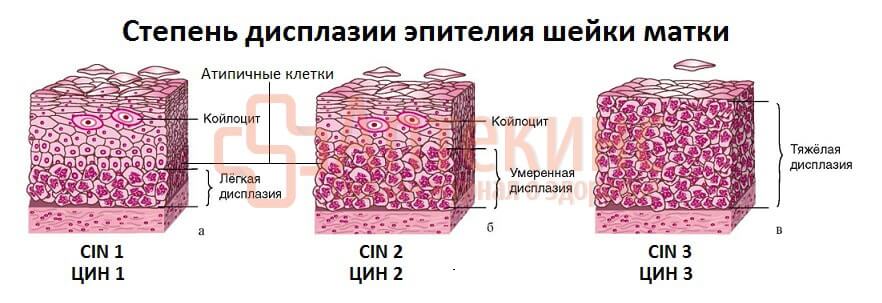
По числу изменённых клеток в мазке, по выраженности атипии (многоядерность, деформация ядра, дистрофия цитоплазмы, др.) можно предположить степень цервикальной дисплазии: ЦИН1 – лёгкая, ЦИН2 – умеренная, ЦИН3 – тяжёлая, СIS – преинвазивная карцинома.
Подробно о ПАП-тесте: как берётся мазок на цитологию, жидкостная цитология, расшифровка цитологии — читайте в статье: Цитология шейки матки – что это такое, расшифровка, атипичные клетки.
Эндоскопическая диагностика ВПЧ 16 типа у женщин
Расширенная кольпоскопия — осмотр оболочек влагалища и шейки матки с помощью оптического прибора кольпоскопа после их обработки химическими веществами (проба с уксусной или салициловой кислотой, проба с раствором Люголя).
При визуализации участков изменённого эпителия пациентка направляется на прицельную биопсию шейки матки. Окончательный диагноз и тактику лечения устанавливают на основании гистологического исследования образца патологической ткани (биоптата).
Если у женщины обнаружено ВПЧ 16 типа – что делать?
Установлено, что присутствие сверхпороговых уровней ДНК ВПЧ у женщин в 99% сопровождается дисплазией эпителия шейки матки (ЦИН) разной степени выраженности.
Порядок действий при ВПЧ-тесте «+» (положительном):
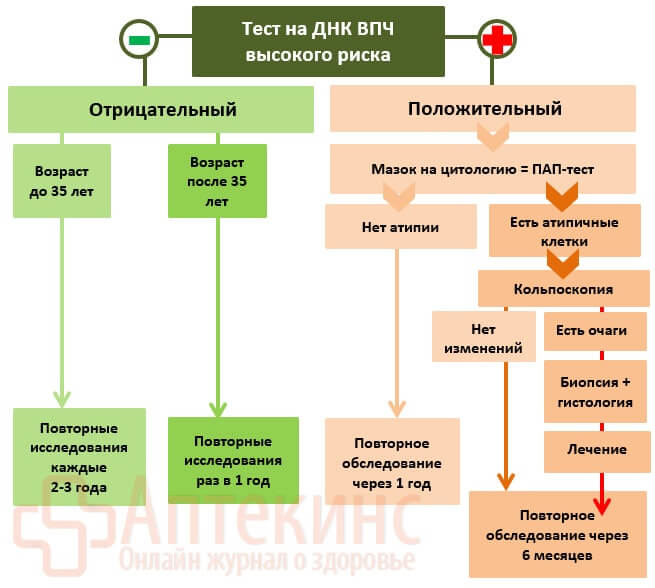
Как лечить ВПЧ 16 у женщин
Медикаментозных, иных средств, для выведения из организма или полного уничтожения ВПЧ 16 не существует .
Поэтому лечение ВПЧ 16/18/… направлено не на искоренение вируса, а на разрушение и удаление поражённых им тканей, на восстановление, укрепление общего и местного иммунитета.
Другими словами, у женщин лечат не ВПЧ 16, а его клинические проявления, болезненные последствия: кондиломы, дисплазию ЦИН, рак шейки матки. Одновременно выявляют и по мере возможности устраняют причины ослабления или дефекта иммунитета.
Местное лечение кондиломатоза:
Физическая или химическая деструкция (разрушение) поражённой ткани:
— криодеструкция;
— лазерное лечение;
— диатермокоагуляция;
— электрохирургическое иссечение;
— Химические методы: солкодерм, трихлоруксусная кислота, подофиллотоксин (требуется консультация врача, есть противопоказания).
Иммунологические методы лечения ВПЧ 16/18/…:
Неспецифическая противовирусная терапия:
— препараты интерферонов а-, β-, γ-;
— препараты-индукторы эндогенного интерферона.
Режим и форму приёма интерферонов назначает врач.
Есть противопоказания и тяжёлые побочные эффекты.
Лечение дисплазии шейки матки (ЦИН):
ЦИН1 – динамическое наблюдение с повторным обследованием каждые 6 мес. Выявление и лечение сопутствующей ИППП. Если дисплазия не регрессирует, проводят криодеструкцию, лазерное лечение или хирургическое иссечение (конизацию) патологической ткани шейки матки.
ЦИН2/3 – лазерное лечение, конизация или ампутация шейки матки.
Сочетание любого варианта ЦИН с миомой, эндометриозом матки — радикальное удаление матки (экстирпация).
Возможно ли самоизлечение от симптомов ВПЧ 16 типа у женщин?
Да. В 50% случаев пороговая вирусная нагрузка, единичные кондиломы, незначительная атипия (КА, ASC-US), лёгкая дисплазия (ЦИН 1) регрессируют и разрешаются без лечения.
Пациенткам с пороговой патологией рекомендуется активное наблюдение, повторное обследование через 3 или 6 месяцев. Важна оптимизация образа жизни: отказ от курения, алкоголя, борьба с лишним весом. При необходимости назначается консультация иммунолога, лечение сопутствующих гинекологических, нейроэндокринных, соматических болезней.
Профилактика ВПЧ 16 типа у женщин
Презерватив не защищает женщину от заражения ВПЧ 16 типа в полной мере.
- Вакцинация (смотрите видео).
- Разумный выбор полового партнёра. Барьерная контрацепция (презерватив) снижает риск заражения ВПЧ.
- Ежегодное диспансерное гинекологическое обследование.
Вероятность заболеть раком шейки матки при «+» тесте на ВПЧ 16 типа
Отметим, что многозначный вопрос происхождения цервикального рака до сих пор не нашёл окончательного решения. Папилломавирусная инфекция – обязательное, но не единственное условие его развития.
Другими словами: все женщины, заболевшие раком шейки матки, были инфицированы ВПЧ высокого риска. Но очень немногие, инфицированные ВПЧ 16/18/… женщины, обязательно заболевают этим раком.
Совокупные риски развития рака шейки матки:
1. Генетическая предрасположенность.
Врождённо высокая чувствительность организма к папилломавирусам. Врождённо-низкий специфичный к ВПЧ противовирусный иммунитет.
2. Заражение инфекцией высокого риска: ВПЧ 16/18/… типов.
3. Вторичный иммунодефицит. Приобретённые дефекты иммунитета, снижение местной или общей резистентности организма.
4. Фоновые заболевания матки: полипы, гиперплазия эндометрия, миома, эндометриоз, кольпиты, цервициты.
5. Травмы шейки матки во время аборта, родов, приводящие к нарушению иннервации и питания цервикальных тканей.
6. Курение.
7. Длительный, неадекватный приём гормональных контрацептивов (КОК).
Нажмите «ЗВЕЗДОЧКУ» сверху 🙂
Источник
Папилломавирус человека (ВПЧ), Human papillomavirus (HPV) принадлежит к семейству паповавирусов (Papovaviridae), роду папилломавирусов. Это ДНК-содержащий мелкий вирус, термостабильный. Является самой распространенной инфекцией, передающейся половым путем: по некоторым данным, в молодом возрасте отмечается инфицирование до 80% населения. Вирус проявляет тропность к эпителию кожи, слизистых оболочек гениталий и других органов (гортань, ротовая полость, слизистая конъюнктивы).
Основной путь передачи — половые контакты, включая анальный, оральный секс, к сожалению, использование презервативов не защищает от инфицирования данным вирусом. Возможна передача при тесном контакте кожи, слизистых оболочек с инфицированными областями. Важным фактором инфицирования новорожденного с последующим развитием респираторного папилломатоза гортани является инфицирование при прохождении по половым путям во время родоразрешения. На сегодняшний день известно более 100 видов вируса папилломы человека (ВПЧ) и из них более 40 могут вызвать поражение аногенитального тракта (половые органы и задний проход) мужчин и женщин и появление остроконечных кондилом. Папилломавирусы можно разделить на 3 основные группы:
неонкогенные ВПЧ (1, 2, 3, 5 генотипы);
низкого канцерогенного риска (НКР) ВПЧ (6, 11, 42, 43, 44 генотипы);
высокого канцерогенного риска (ВКР) ВПЧ (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 и 68 генотипы).
ВПЧ низкого канцерогенного риска (ВПЧ НКР): группа вирусов, которая приводит к доброкачественным поражениям, представлена 5 генотипами, но основными являются 6 и 11, которые составляют до 90% всех случаев инфицирования данными вирусами. Наиболее частые клинические проявление ВПЧ НКР- это остроконечные кондиломы (Condylomata acuminata). Также выделяют еще разновидности остроконечных кондилом: кератотические бородавки с локализацией на сухой коже, папулезные бородавки с локализацией на полностью ороговевшем эпителии, гигантская кондилома Бушке-Левенштейна (встречающаяся у больных сниженным клеточным иммунитетом или при беременности). Эндоуретральные кондиломы локализуются в уретре, часто сочетаются с обычными кондиломами и встречаются преимущественно у мужчин. Кондиломы шейки матки часто сочетаются с генитальными кондиломами: экзофитные кондиломы, эндофитные (плоские).
ВПЧ высокого канцерогенного риска (ВПЧ ВКР): группа типов высокого канцерогенного риска представлена 15 генотипами, наиболее распространенными из которых являются десять: 16, 18, 31, 33, 35, 39, 45, 52, 58, 59. При этом на долю 16 и 18 типов приходится 70% всех случаев инфицирования, и именно данные типы характеризуются высоким канцерогенным потенциалом, в отношении 18 генотипа наблюдается высокая частота выявления при аденокарциномах. На сегодняшний день доказана роль ВПЧ в развитии рака шейки матки, большей доли рака заднего прохода (около 90% случаев), около 40% всех случаев рака влагалища, вульвы, полового члена, 10–15% случаев рака ротовой полости и гортани.
Вирусная ДНК способна персистировать в клетке в двух формах: эписомальной (продуктивная стадия) и интегрированной (интегрированная стадия). На эписомальной стадии происходит усиленная продукция новых вирусов, что способствует вовлечению в патологический процесс новых клеток, однако клетки не теряют контроль над процессами апоптоза и эта стадия характеризуется доброкачественными изменениями со стороны эпителия. Интегрированная стадия — это стадия, когда вирус встраивается в геном клетки и приводит к суперэкспрессии онкобелков Е6, Е7, ассоциируется с предраковыми изменениями и требует соответствующей тактики лечения пациента.
Инфекция, вызываемая вирусом папилломы человека, имеет ряд важных особенностей, без учета которых использование ВПЧ-тестирования сопряжено с рядом трудностей в трактовке результатов.
С одной стороны:
ВПЧ является самой распространенной ИППП (до 80% лиц молодого возраста инфицированы данным вирусом);
при инфицировании большинство женщин (около 80%) излечиваются от ВПЧ в течение 9–15 месяцев от момента заражения без проведения лечебных процедур (т. е., при повторении теста на генотипирование через год возможно исчезновение выявленного ранее генотипа ВПЧ или изменение спектра генотипов). С возрастом способность к самоэлиминации значительно снижается;
инфицирование ВПЧ и заболевание — НЕ СИНОНИМЫ! Инфекция приводит к развитию предрака у малой части инфицированных женщин (около 0,5%);
от заражения до развития предрака и РШМ, в среднем, проходит 10–20 лет. С возрастом способность к элиминации вируса снижается, соответственно, повышается риск развития предрака и рака;
отсутствуют эффективные методы лечения на стадии латентной инфекции (нет изменений в цитологической и/или кольпоскопической картине, но выявляется вирус).
С другой стороны:
ВПЧ является основной причиной рака шейки матки. Инфицированные женщины имеют в 300 раз более высокий риск развития рака. Разработаны не только методы вторичной профилактики (цервикальный скрининг для выявления предраковых стадий), но и первичной — вакцинация девочек и мальчиков в возрасте 9–12 лет;
инфекция коварна и довольно часто не вызывает никаких жалоб у пациента и не выявляется при осмотре до перехода в стадию инвазивного рака;
клинические проявления папилломавирусной инфекции высокого риска могут маскироваться другими заболеваниями урогенитального тракта, что не позволяет вовремя выявить их с использованием традиционных методов.
Из перечисленных особенностей папилломавирусной инфекции следует, что:
1. Положительный результат тестирования на наличие вируса должен трактоваться как:
принадлежность пациента к группе высокого риска по развитию рака шейки матки;
потребность в дополнительных тщательных диагностических процедурах для выяснения текущей стадии инфекции, исключения тяжелой дисплазии и рака шейки матки;
необходимость в наблюдении за инфекцией (персистенцией) при отсутствии клинических или субклинических проявлений.
2. Отрицательный результат тестирования трактуется как отсутствие риска развития тяжелой дисплазии и рака.
Лабораторная диагностика. Диагностика ВПЧ инфицирования определяется клиническими проявлениями и клиническими задачами прогноза риска развития ВПЧ-ассоциированных злокачественных новообразований.
Лабораторные методы диагностики ВПЧ инфекции:
прямые методы: оценка наличия койлоцитов в цитологических мазках (низкая диагностическая чувствительность); выявление наличия маркеров пролиферации р16/ki 67; молекулярные методы (ПЦР анализ), которые проводятся в формате качественного и количественного тестирования с возможностью генотипирования, определение генотипов НКР и ВКР ВПЧ;
серологические методы не используются для диагностики ВПЧ инфекции.
Стратегии использования ВПЧ-тестов в диагностике предрака и рака шейки матки:
входит в комплекс цервикального скрининга: в качестве теста сортировки патологических ПАП тестов у женщин до 30 лет; тест совместно с цитологическим исследованием для всех женщин старше 30 лет. В данном случае наличие инфицирования ВПЧ (особенно, 16 и 18 генотипом, с высокой вирусной нагрузкой) позволяет прогнозировать высокий риск наличия или развития РШМ, что определяет необходимость дополнительных обследований. В случае отрицательных результатов ВПЧ тестирования, периодичность скрининга может быть увеличена до 3–5 лет (в разных странах действуют различные рекомендации) при условии отсутствия изменений в цитологическом исследовании;
рекомендован в некоторых странах как тест первичного скрининга на РШМ у женщин старше 30 лет;
контроль эффективности лечения дисплазий (первое исследование проводится через 6 месяцев после лечения совместно с ПАП тестом). При этом в случае получения положительных результатов ВПЧ теста и нормальной цитологии, необходимо дополнительное обследование, т. к. риск наличия или развития патологии высокий.
Различные методы молекулярной диагностики (ПЦР анализа) позволяют решить различные диагностические задачи:
качественный формат позволяет выявить наличие инфицирования, однако не позволяет оценить клинически значимые количества вируса, которые ассоциируются с высоким риском наличия предраковых поражений;
количественный формат позволяет выявить вирус, определить вирусную нагрузку. Это позволяет оценить не только степень риска, но и возможное уже наличие предраковых изменений, т. к. высокая вирусная нагрузка ассоциируется с реализацией онкогенного потенциала вируса. При правильном и стандартизированном заборе клинического материала вирусная нагрузка менее 105 геномных эквивалентов (ГЭ) ВПЧ ВКР в соскобе (Josefsson et al, 2000; van Duin et al, 2002; Dalstein et al, 2003; Snijders et al, 2003; Moberg et al, 2004, 2005) или 103 ГЭ приходящихся на 100 тыс. клеток человека считается клинически малозначимой, так как практически не встречается при тяжелой дисплазии и РШМ, а также ассоциирована с минимальным риском их развития. Напротив, количество вируса более 105 ГЭ, приходящихся на 100 тыс. клеток при установленном факте персистентного течения инфекции (ВПЧ выявляется более 1 года), обозначается как повышенная нагрузка ВПЧ и ассоциировано с повышенным риском развития тяжелой дисплазии и чаще встречается при РШМ. Наконец, определенной информацией обладает мониторинг вирусной нагрузки. Так, считается, что снижение количества ДНК ВПЧ более чем на 1 lg может являться маркером транзиторной инфекции. Рост вирусной нагрузки через 3, 6 и 9 мес. после проведенного лечения свидетельствует о возможности рецидива.
Генотипирование ВПЧ дает дополнительные возможности определения прогноза течения заболевания. Необходимость генотипирования может быть оправдана, т. к.:
выявление нескольких генотипов вируса ассоциировано с менее благоприятным прогнозом течения заболевания и более высоким риском персистенции;
степень онкогенности различных генотипов высокого риска не одинакова. Наибольшей онкогенностью обладают 16 и 18 типы ВПЧ, существуют рекомендации по проведению определения этих двух генотипов вируса после теста на широкий спектр типов с целью более агрессивной тактики ведения пациентов: при выявлении 16 и 18 генотипов рекомендуется сразу проводить кольпоскопическое обследование, при выявлении других типов высокого риска — сначала проводить цитологию, и только при положительном результате цитологии проводить кольпоскопию;
проведение генотипирования позволяет отличить реинфицирование от персистирования инфекции при повторном визите пациента. Получать подобную информацию тем более важно, так как опасность представляет именно хроническая персистентная форма инфекции, недавнее же инфицирование, наиболее вероятно, спонтанно излечивается. О реинфицировании говорит изменение спектра генотипов, о персистирующей инфекции — сохранение генотипа вируса через год после первого тестирования; повторное инфицирование тем же генотипом вируса после самостоятельного излечения практически невозможно.
Источник

