Мутация braf при меланоме стоимость
BRAF мутация при раке
Эффективность лечения пациента с диагностированным раком во многом зависит от результатов генетических исследований. При обнаружении молекулярных механизмов возникновения опухоли рациональные терапевтические методы воздействия на злокачественное образование позволяют значительно улучшить качество и продолжительность жизни пациента.
Изменения в гене BRAF характерны для нескольких типов онкологических заболеваний. Системные нарушения гена происходят на уровне передачи сигналов. Мутировавшая часть ДНК запускает неконтролируемый процесс деления клеток, который и приводит к образованию опухоли.
BRAF мутация встречается при раке кожи, колоректальном раке, немелкоклеточных опухолях легких и некоторых видах злокачественных образований щитовидной железы. В качестве блокаторов сигнального каскада используются низкомолекулярные ингибиторы фермента. Они предотвращают деление клеток и разрастание опухолевой ткани.
Методы определения мутации
Основным способом исследования в лаборатории Центра Инновационных Биотехнологий Аллель является пиросеквенирование. Данный метод позволяет выявить различные виды мутаций в исследуемом образце, что помогает врачу подобрать оптимальный способ лечения для каждого конкретного пациента.
Материалом для проведения анализа служит ДНК опухолевой ткани. Биоптат новообразования помещается в парафиновый блок или передается в емкости со специальным раствором, из которого изготавливаются блоки для долгосрочного хранения и возможности проведения других исследований.
Мутация гена BRAF V600E
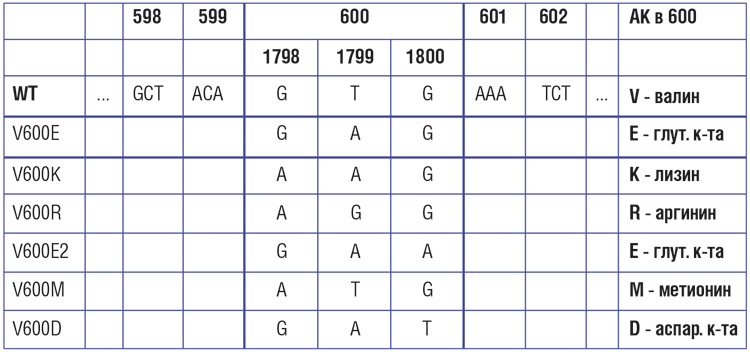
Наиболее частые изменения происходят в кодоне 600 15-го экзона. При этом виде мутации привычная аминокислота валин заменяется на другую. Мутация именуется V600E, последняя буква в названии означает аминокислоту, заменяющую валин.
Изменения в BRAF V600E характерны для меланомы, его обнаруживают у подавляющего большинства пациентов (40-70%). В случае такой мутации в кодоне 600 аминокислота валин заменяется на глутаминовую кислоту. Структурное изменение ДНК этого типа является доминирующим и встречается в 60-90% случаев меланомы.
Рекомендации российского общества клинической онкологии предлагают эффективные варианты лечения для пациентов с BRAF мутацией V600E.
BRAF мутация при меланоме
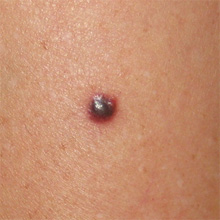
Меланома – разновидность рака кожи, зарождающаяся в пигментных клетках меланоцитах. Большая часть новообразований проявляется спорадически, однако некоторые виды меланомы могут развиваться в родинках.
Отличительной особенностью меланом являются неровные края и неправильные формы. Размер новообразования может варьироваться от нескольких миллиметров до нескольких сантиметров в диаметре. Они могут иметь разное окрашивание – черные, коричневые, красные, синие и белые.
Меланома возникает на коже, но может затрагивать и другие ткани. Достаточно распространена увеальная меланома (поражение оболочки глаз), а также опухоль в слизистых оболочках, выстилающих различные органы человека.
Новообразования влияют только на эпидермис, но глубокое прорастание в несколько слоев кожи может стать причиной метастазирования на другие участки тела.
Опухоли чаще всего обнаруживаются на спине у мужчин и на ногах у женщин. Средний возраст развития заболевания – от 50 до 70 лет и все чаще встречается у молодого населения. Пигментированные кожные образования, а также родинки влияют на риск возникновения меланомы. Риск повторного развития новообразований у людей, ранее страдавших таким недугом в несколько раз больше, чем у пациентов с прежде не диагностированным заболеванием. Больные с меланомой выживают в 90% случаев.
Мутацию гена c-KIT выявляют у 15% больных. Такой маркер характерен для заболевания, затрагивающего слизистые оболочки гениталий, прямой кишки, носовых ходов и полости рта. Изменение также выявляется при меланоме, расположенной на ладонях и ногтях.
При выявлении c-KIT мутации при меланоме назначают для терапии препараты-ингибиторы c-KIT. В 30% случаев лечение имеет положительный эффект.
Сколько стоит анализ BRAF мутации при меланоме
Центр Инновационных Биотехнологий Аллель предлагает широкий спектр генетических исследований. В лаборатории, где можно сделать анализ мутации генов BRAF и c-KIT, используется точный и достоверный метод исследования – пиросеквенирование. Для диагностики необходимо предоставить образец опухолевой ткани. Уточнить детали заказа, узнать стоимость и оставить заявку можно на сайте, заполнив короткую форму, или позвонив по телефону: +7 (495) 780-92-96.
Источник
- Частота и виды мутаций в гене BRAF
- Cтатус мутации гена BRAF и выбор тактики лечения
Частота и виды мутаций в гене BRAF
Частота мутаций в гене BRAF при меланоме кожи, по данным разных исследователей, варьирует от 30-40% до 70%. Наиболее распространенной (69-94% случаев) разновидностью BRAF-мутаций является V600E – замена валина на глутамин в 600-м кодоне. Эта мутация представляется доминирующей, но далеко не единственной разновидностью нарушений BRAF [14, 15]. Второй по частоте является мутация V600К – ее частота может достигать 5-10%. Мутации V600D и V600R встречаются значительно реже.
Cтатус мутации гена BRAF и выбор тактики лечения
За последние годы достигнуты значительные успехи в изучении патогенетических основ развития меланомы и сделан огромный шаг к выявлению новых потенциальных молекулярных мишеней. Открытие молекулярной мишени BRAF и понимание ее роли в патогенезе меланомы легли в основу разработки нового класса препаратов – низкомолекулярных ингибиторов мутированного фермента BRAF. Использование этих препаратов позволяет блокировать патологически активированный сигнальный каскад, который запускается мутацией BRAF V600, и, таким образом, тормозить развитие опухоли. Следует особо отметить, что воздействие данной группы препаратов на опухолевые клетки с нормальной последовательностью BRAF, напротив, может сопровождаться патологической активацией каскада RAS-RAF-MEK-ERK и провоцировать рост меланомы. Этот феномен свидетельствует об исключительной важности достоверной диагностики статуса гена BRAF.
BRAF ингибиторы не должны использоваться в тех случаях, когда статус мутации BRAF не определен или мутация не обнаружена!
Следует подчеркнуть, что ингибиторы BRAF и MEK зарегистрированы к применению только для терапии метастатической формы меланомы. В настоящее время отсутствуют данные по использованию ингибиторов BRAF и MEK в адъювантном режиме, поэтому они не могут быть рекомендованы пациентам, перенесшим (условно-)радикальное удаление первичной меланомы и метастических очагов.
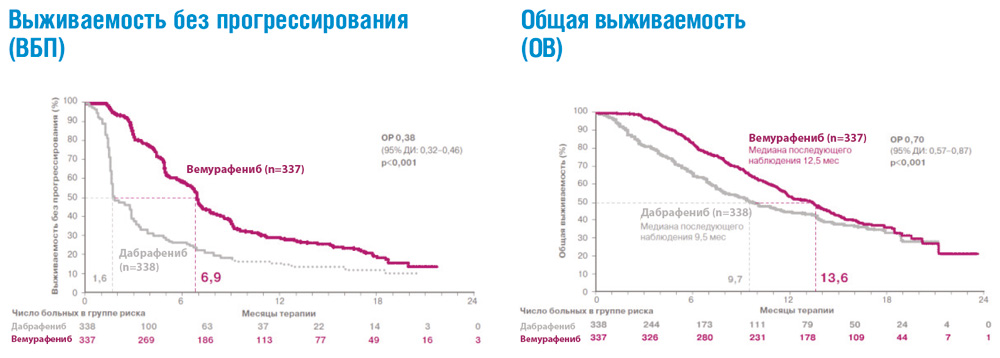
В рандомизированных клинических исследованиях ингибиторы BRAF – вемурафениб и дабрафениб – продемонстрировали значительное преимущество по сравнению со стандартной химиотерапией в отношении частоты объективных ответов, продолжительности жизни без прогрессирования и общей продолжительности жизни у пациентов с метастатической меланомой и подтвержденной мутацией гена BRAF, ранее не получавших системного лечения (см. рис. 2). Полученные результаты привели к пересмотру международных клинических рекомендаций, которые включили эти препараты в современные стандарты лечения метастатической меланомы кожи с BRAF мутацией.
Результаты последних исследований показали, что двойное ингибирование сигнального пути MAРK, которое достигается при одновременном использовании ингибиторов BRAF и MEK, обладает более высокой эффективностью по сравнению с ингибитором BRAF в монорежиме. Важно отметить, что помимо более высокой эффективности комбинация препаратов снижает вероятность развития резистентности к проводимой терапии и отдельных нежелательных явлений, в том числе плоскоклеточного рака кожи. В рамках клинического исследования coBRIM было подтверждено, что комбинированная терапия с использованием препаратов вемурафениб и кобиметиниб в 90% случаев позволяет достичь ответа на терапию у больных BRAF+ метастатической меланомой. У каждого второго пациента более года отсутствовали признаки прогрессирования заболевания, а общая выживаемость приближалась к 2 годам (рис. 3).
Сходные результаты были продемонстрированы в исследованиях дабрафениба и траметиниба. В частности, исследование COMBI-V (дабрафениб+траметиниб vs монотерапия вемурафенибом) продемонстрировало значимой увеличение общей продолжительности жизни у пациентов, получавших комбинированную терапию, по сравнению с применением вемурафениба без ингибитора MEK (25.6 мес. vs 18 мес.; рис. 4, табл. 1). В клиническом испытании COMBI-D сравнивалась эффективность комбинации дабрафениб+траметиниб по отношению к монотерапии дабрафенибом в сочетании с плацебо. Примечательно, что в этом исследовании были зарегистрированы практические идентичные показатели общей продолжительности жизни (25.1 мес. vs 18.7 мес.; рис. 5, табл. 1).
Определение статуса гена BRAF является обязательным компонентом выработки тактики лечения всех пациентов с неоперабельной/метастатической меланомой кожи.

Рисунок 2. Результаты рандомизированного исследования BRIM-3: сравнение эффективности вемурафениба и дабрафениба в 1-й линии терапии метастатической меланомы с мутацией BRAF.
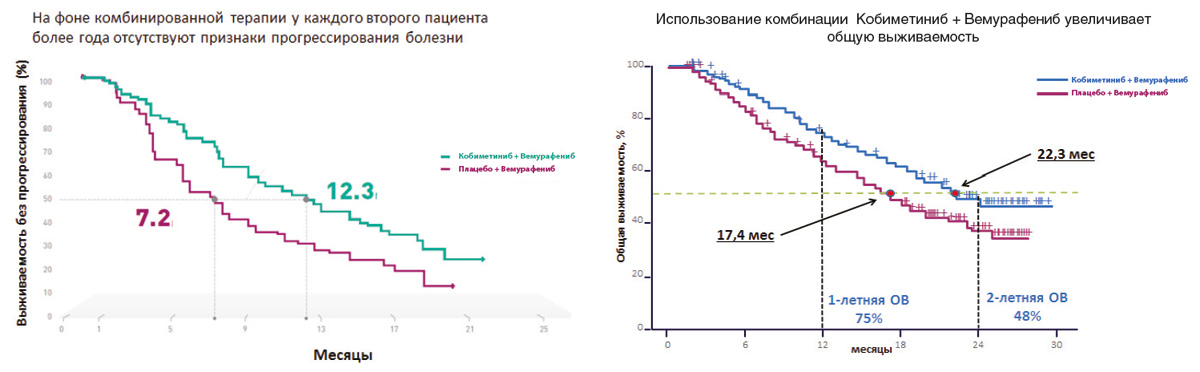
Рисунок 3. Результаты рандомизированного исследования coBRIM: сравнение эффективности комбинации кобиметиниба+вемурафениба и вемурафениба+плацебо в 1-й линии терапии метастатической меланомы с мутацией BRAF.
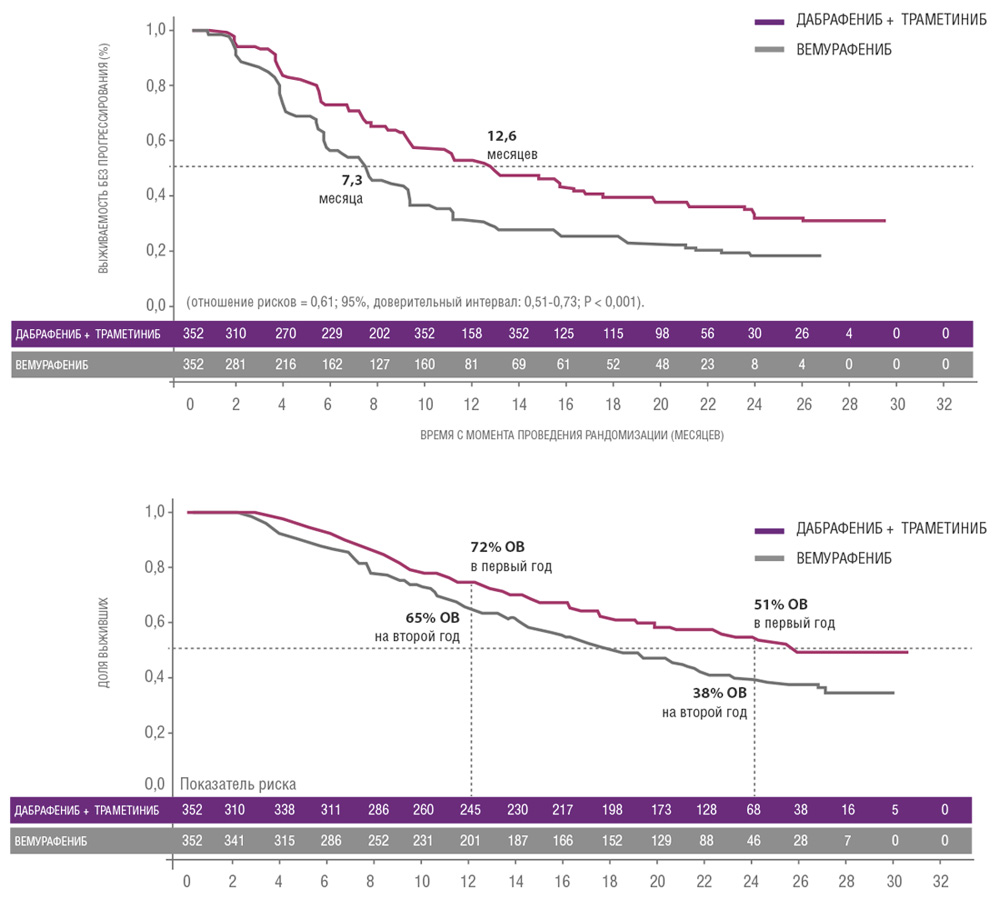
Рисунок 4. Результаты клинического исследования COMBI-V: (дабрафениб+траметиниб vs монотерапия вемурафенибом).
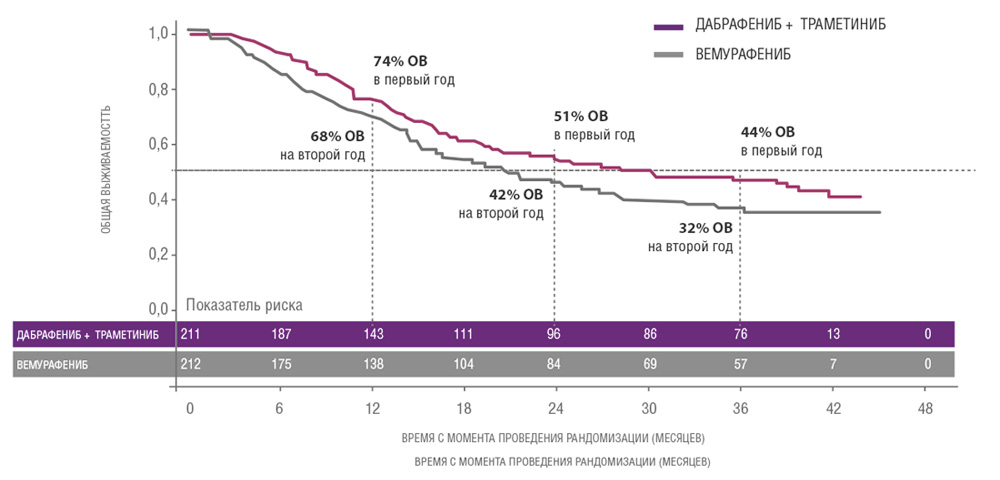
Рисунок 5. Результаты клинического испытания COMBI-D: эффективность комбинации дабрафениб+траметиниб по отношению к монотерапии дабрафенибом в сочетании с плацебо.
Сводные данные по всем исследованиям представлены в таблице 1.
| Исследование | COMBI-d | COMBI-v | ||
|---|---|---|---|---|
| Препарат(ы) | Д + T | Д + пла | Д + T | В |
| Кол-во пациентов, n | 211 | 212 | 352 | 352 |
| Медиана ВБП, мес. | 11,0 | 8,8 | 12,6 | 7,3 |
| Медиана ОВ, мес. | 25,1 | 18,7 | 25,6 | 18,0 |
| Медиана ОВ, ЛДГ≤ВГН | Нет анализа | НД | 21,5 | |
| Медиана ОВ, ЛДГ>ВГН | 10,8 | 8,9 | ||
Сокращения: В – вемурафениб, К – кобиметиниб, Д – дабрафениб, Т- траметиниб, пла – плацебо, НД – не достигнута, ВГН – верхняя граница нормы.
Таким образом, использование BRAF/MEK ингибиторов у пациентов с мМК, имеющей BRAF мутацию, представляет первый успешный пример персонализированной терапии, изменившей представление о мМК как об опухоли, рефрактерной к лекарственному лечению. Эти препараты пришли на смену химиотерапии и стали новым стандартом лечения меланомы с BRAF мутацией, что подтверждает ранее сформулированный постулат о необходимости разработки различных подходов к лечению для различных молекулярно-генетических подтипов меланомы. Появляются результаты исследований таргетных препаратов и при других типах меланомы, имеющих альтернативные мутации (NRAS, cKIT). Можно ожидать, что определение молекулярно-генетического портрета опухоли уже в ближайшее время станет неотъемлимой частью разработки стратегии лечения каждого пациента, имеющего диагноз «меланома».
На сегодняшний день все существующие BRAF и MEK ингибиторы зарегистрированы на территории Российской Федерации и, при соответствующем лекарственном обеспечении, с успехом могут быть использованы для терапии мМК. Профиль безопасности этих препаратов позволяет использовать их в амбулаторных условиях.
Статьи:
- Г.Ю. Харкевич. Вемурафениб в лечении метастазов меланомы в головной мозг. Онкология. Журнал им. П.А. Герцена, 6, 2014.
- Г.А. Франк et al, Первое Всероссийское молекулярно-эпидемиологическое исследование меланомы: результаты анализа мутаций в гене BRAF. Архив Патологии, 3, 2014.
- С.А. Проценко et al, Современные возможности персонализированной терапии метастатической меланомы кожи. Современная онкология №3, том 16, 2014.
- Larkin J et al. Update of progression-free survival and correlative biomarker analysis from coBRIM: Phase 3 study of cobimetinib plus vemurafenib in advanced-BRAFmutated melanoma; Poster presentation at ASCO 2015.
- Robert C, et al. Ann Oncol. 2015; 26 (suppl 6) [abstract 3301].
- Flaherty K, et al. J Clin Oncol. 2016; 34 (suppl; abstr 9502).
- Hauschild A, et al. Poster presented at ESMO 2014, Abstract 1092PD.
- Robert, C. LBA4 Oral presentation at ESMO 2015.
Источник

В норме ген BRAF вместе с факторами роста и гормонами участвует в регуляции деления клеток за счет активации специфического сигнального пути. Если же его структура изменяется, то процесс деления выходит из-под контроля. Мутации в гене BRAF выявляются при различных видах рака, однако на первом месте в списке онкологических заболеваний стоит меланома. Определить статус гена при данной болезни крайне важно, так как от этого будет зависеть дальнейшая тактика лечения.
Частота и виды мутаций BRAF
По данным разных авторов, BRAF мутация встречается от 30% до 70% пациентов, которым поставлен диагноз «меланома». При этом изменения в гене могут быть самыми разнообразными. Всего известно более 40 BRAF мутаций, но наиболее часто (около 90% всех случаев) выявляется замена аминокислоты валина на аминокислоту глутамина в кодоне 600. Соответственно, такая мутация называется BRAF V600E. Второе по популярности изменение в гене при меланоме – это замена аминокислоты валина на аминокислоту аспарагин в том же кодоне. Такая мутация обозначается V600K.
Методы диагностики
Выявить мутации BRAF можно при помощи молекулярно-генетических методов диагностики. Для проведения исследования необходим образец тканей меланомы кожи, в которых содержится не менее 20% опухолевых клеток. Как правило, такой материал поступает в лабораторию после удаления, после чего он фиксируется в формалине и заключается в парафиновые блоки. Перед определением мутаций необходимо выполнить пробоподготовку. Материал извлекается из парафина, затем выполняется процесс экстракции ДНК, которая исследуется.
Базовым методом, который позволяет выявить мутации в гене BRAF, является полимеразная цепная реакция (ПЦР). Это исследование является относительно простым и дешевым, обладает хорошей чувствительностью и специфичностью, однако имеет существенный недостаток. Один анализ позволяет определить только одну мутацию BRAF. Если же стоит задача выявить несколько мутаций, то исследование придется повторять.
Более совершенным считается секвенирование, при помощи которого можно установить точную последовательность ДНК целого гена. Данный метод более затратный и требует дорогостоящего оборудования, но при этом он позволяет одновременно выявить все мутации в гене BRAF за одно исследование. Среди недостатков секвенирования можно отметить риск получить ложноотрицательный результат (выявляется в 2%-10% случаев) из-за присутствия в материале большого количества нормальных клеток с неизмененной ДНК.
Зачем определять BRAF мутацию при меланоме
Определение мутации в гене BRAF имеет важное значение при подборе лечения меланомы. Одним из современных методов является таргетная терапия, которая направлена на устранение конкретного механизма образования опухолевых клеток. В случае с меланомой применяются ингибиторы мутированного фрагмента гена BRAF, которые прерывают цепочку биохимических реакций и не дают опухоли развиваться дальше. При назначении таких препаратов определение статуса гена BRAF должно проводиться в обязательном порядке. При отсутствии мутации дорогостоящее лечение окажется неэффективным, а в некоторых случаях может и ускорить прогрессирование опухолевого процесса.
Препараты из группы ингибиторов BRAF могут применяться только при лечении метастатической меланомы. При этом не изучена эффективность лечения в адъювантном режиме, поэтому такие препараты не назначают пациентам, у которых выполнялось хирургическое удаление опухоли или метастазов, а также химио- и лучевая терапия.
Первыми зарегистрированными препаратами из группы ингибиторов BRAF, которые начали применяться при лечении метастатической и неоперабельной меланомы, стали вемурафениб и дабрафениб. При проведении клинических испытаний, они показали очень хорошие результаты. В настоящее время применяется комбинированное лечение меланомы, при котором, кроме ингибиторов BRAF назначаются ингибиторы МЕК. Такое сочетание позволяет максимально замедлить прогрессирование заболевания и увеличить продолжительность жизни пациентов.
Несмотря на большие успехи в лечении меланомы, все еще остаются нерешенными несколько проблем. Во-первых, отсутствуют эффективные методы терапии, которые можно применять при отсутствии мутаций в гене BRAF. Во-вторых, при назначении ингибиторов BRAF у пациентов спустя некоторое время развивается устойчивость к такому лечению, и меланома начинает снова прогрессировать.
Запись
на консультацию
круглосуточно
Источник
Меланома — одна из самых агрессивных и опасных опухолей. Она рано распространяется на близлежащие лимфатические узлы и дает метастазы в различные органы.
Распространенность меланомы постоянно растет во всем мире, в том числе и в России. Еще совсем недавно наличие метастазов и невозможность удалить опухоль хирургическим путем означали для больного неминуемую смерть.
В последние годы появились новые эффективные препараты, которые помогают увеличить выживаемость пациентов с меланомой на поздней стадии. Одно из наиболее перспективных современных направлений — иммунотерапия.

Клетки с поврежденными генами, способные давать рост злокачественной опухоли, постоянно образуются в организме любого человека. Но иммунная система вовремя находит и уничтожает их. Когда количество переродившихся клеток достигает определенной критической величины, защитные механизмы перестают адекватно работать. Иммунные клетки не реагируют на опухоль, не атакуют её.
Задача иммунотерапии — активировать иммунную систему, снять имеющиеся блоки, запустить процесс распознавания и уничтожения опухолевых клеток. Сегодня для этого используются моноклональные антитела — вещества, которые воспринимают определенные молекулы в качестве антигенов, связываются с ними, тем самым активируя иммунные клетки. Названия всех таких препаратов имеют окончание «-маб» (от англ. monoclonal antibody — «моноклональное антитело»):
- Кейтруда – Пембролизумаб
- Опдиво – Ниволумаб
- Ервой – Ипилимумаб
- Зелбораф – Вемурафениб
- Тафинлар – Дабрафениб
Также эффективными средствами для борьбы с меланомой на поздних стадиях являются ингибиторы BRAF — белка, который образуется в результате мутации в одноименном гене и запускает процесс бесконтрольного размножения клеток. Поговорим о каждом из этих препаратов подробнее.
Кейтруда
Кейтруда (другие названия: Пембролизумаб, MK-3475) — инновационный препарат, который был одобрен FDA (Американским управлением по надзору за качеством пищевых продуктов и медикаментов) в сентябре 2014 года, и в настоящее время уже достаточно широко применяется для лечения меланомы на поздних стадиях.
В 2014 году Кейтруда получила статус «приоритетное рассмотрение» и «прорыв в медицине». Это означает, что Пембролизумаб был включен в группу лекарственных средств, способных повысить эффективность и безопасность лечения редких и серьезных заболеваний. Именно поэтому препарат был так быстро одобрен и внедрен в клиническую практику. Обычно это происходит намного дольше.
Как действует Кейтруда?
Препараты для иммунотерапии меланомы и других злокачественных опухолей существуют уже достаточно давно. Но они всегда имели низкую эффективность, и до недавнего времени ученые не знали, как справиться с этой проблемой.
Задача иммунотерапии — активировать иммунную систему больного, заставить её атаковать и уничтожать раковые клетки. Долгое время препятствием для достижения этой цели становился белок PD-1. Это иммуноглобулин, молекулы которого встроены в клеточные мембраны. Он играет роль в дифференцировке иммунных клеток.
Белок PD-1 блокирует работу иммунной системы. Он не дает Т-лимфоцитам распознавать и уничтожать раковые клетки.
Кейтруда содержит моноклональные антитела, которые блокируют PD-1. Препарат помогает убрать «тормоз», благодаря чему лимфоциты приобретают способность атаковать опухолевую ткань.
Когда применяется этот препарат?
Показания к применению Кейтруды:
- метастазирующая меланома на поздних стадиях;
- неоперабельная меланома;
- отсутствие эффекта от лечения другими препаратами.
Насколько эффективна Кейтруда?
В Калифорнийском Университете в Лос-Анджелесе было проведено исследование, в котором приняли участие 173 человека с диагностированной прогрессирующей меланомой. Их разделили на две группы. В одной из них пациенты получали стандартную дозу препарата 2 мг на килограмм массы тела через каждые 3 недели. Во второй группе доза была увеличена в 5 раз (10 мг/кг).
У 24% пациентов, получавших препарат в дозе 2 мг/кг, опухоль уменьшилась более чем на треть. Повторный рост меланомы не отмечался, а эффект препарата сохранялся от 1,4 до 8,5 месяцев (в отдельных случаях — дольше).
Безопасна ли Кейтруда?
Второе исследование было проведено с участием 411 пациентов, которые имели прогрессирующую меланому и принимали Кейтруду. При этом тяжелые побочные эффекты со стороны кишечника, легких и печени отмечались редко.
Чаще всего у больных возникали такие побочные эффекты, как повышенная утомляемость, кашель, тошнота, сыпь, кожный зуд, снижение аппетита, запор, диарея, боли в суставах (источник данных об исследованиях — https://www.medicalnewstoday.com/articles/282101.php).
Опдиво
Опдиво (другое название — Ниволумаб) — препарат из группы моноклональных антител, одобренный FDA в конце декабря 2014 года.
В 2014 году этот препарат получил статусы: «принципиально новое лекарственное средство», «орфанный препарат», «ускоренное рассмотрение». Ниволумаб, так же, как и Кейтруда, был одобрен по ускоренной процедуре.
Как работает Опдиво?
По механизму действия препарат представляет собой аналог Кейтруды. Он блокирует рецептор PD-1, который снижает активность Т-лимфоцитов, не дает им распознавать и атаковать иммунные клетки.
В каких случаях планируется применять Ниволумаб?
Показания к применению препарата:
- прогрессирующая неоперабельная меланома;
- отсутствие эффекта от лечения Ипилимумабом;
- меланома, при которой имеется мутация гена BRAF, но применение ингибиторов BRAF не приносит эффекта.
Насколько эффективен Ниволумаб?
Эффективность Опдиво была изучена во время исследования, в котором приняли участие 120 больных с неоперабельной метастатической меланомой. В ходе применения препарата у 32% пациентов отмечалось существенное уменьшение размеров опухоли. Эффект сохранялся в течение 6 месяцев.
Безопасность
Также было проведено исследование, во время которого оценивалась безопасность препарата. 268 больных получали Ниволумаб, 120 — классическую химиотерапию.
Наиболее распространенные побочные эффекты, отмечавшиеся у больных, принимавших Опдиво: зуд, кожная сыпь, инфекции верхних дыхательных путей, кашель, задержка жидкости в организме (отеки).
Редко отмечаются тяжелые нарушения со стороны легких, толстой кишки, печени, почек и желез внутренней секреции. Эти побочные эффекты связаны с действием препарата на иммунитет (источник данных об исследованиях — https://www.medicalnewstoday.com/releases/287399.php).
Ервой
Ервой (другие названия — Ипилимумаб, MDX-010, MDX-101) — препарат для лечения меланомы на поздних стадиях, одобренный FDA в марте 2011 года.
Ипилимумаб в настоящее время широко применяется для лечения метастазирующих и неоперабельных меланом на поздней стадии.
Как действует Ервой?
Как и другие препараты из группы моноклональных антител, Ипилимумаб действует не на саму опухоль, а на иммунную систему. Организм начинает самостоятельно уничтожать переродившиеся раковые клетки.
На поверхности иммунных клеток, — Т-лимфоцитов, — находится особый рецептор CTLA-4. Ипилимумаб, являясь антителом, воспринимает этот рецептор как антиген и присоединяется к нему, тем самым активируя лимфоцит.
При применении Ервоя пятилетняя выживаемость больных достигает 16%. Препарат обладает эффективностью 80% и более: это проявляется в уменьшении размеров метастазов, снижении раковой интоксикации, повышении качества жизни. Ервой дает более медленный эффект, чем Зелбораф и другие ингибиторы BRAF (см. ниже). Но он действует более продолжительно.
В большинстве случаев препарат переносится пациентами хорошо. Возможны побочные эффекты, такие как: общее недомогание, высыпания на коже, жидкий стул.
Редко встречаются более тяжелые поражения кожи, слизистых оболочек, печени, периферических нервов, эндокринных желез
Зелбораф
Зелбораф (Вемурафениб) — препарат из группы ингибиторов BRAF, применяемый для иммунотерапии метастазирующей меланомы на поздних стадиях. Он был одобрен FDA в августе 2011 года, а Европейским агентством лекарственных средств — в 2012 году.
Механизм действия. Что такое ингибиторы BRAF?
Зелбораф стал первым препаратом для лечения меланомы из группы ингибиторов BRAF.
BRAF — ген, который кодирует одноименный белок-фермент. Он обеспечивает размножение клеток под контролем гормонов и факторов роста.
В результате мутации гена BRAF происходят нарушения:
- избыточное деление клеток;
- ошибочная устойчивость клеток к апоптозу — запрограммированной естественной гибели.
Это приводит к возникновению раковой опухоли. Вемурафениб блокирует белок BRAF. Препарат действует очень быстро: после начала приема таблеток размеры опухоли обычно существенно уменьшаются в течение месяца. Одновременно нормализуется состояние больного, уменьшается раковая интоксикация.
Показания к применению
Зелбораф применяется для лечения меланомы на поздних стадиях. Препарат эффективен только в том случае, если у больного имеется мутация гена BRAF. Если же в клетках меланомы этот ген нормален, то препарат может, напротив, ускорить рост опухоли.
Поэтому перед назначением Вемурафениба всегда проводится молекулярно-генетическое исследование. Сегодня FDA одобрен инновационный тест THxID BRAF Kit, разработанный компанией bioMérieux.
Дабрафениб
Дабрафениб (Тафинлар) — новый препарат для иммунотерапии меланомы на поздней стадии, относящийся к группе ингибиторов белка BRAF. Он был одобрен FDA в 2014 году.
Как действует Тафинлар?
Дабрафениб, как и Зелбораф, блокирует белок, который образуется в результате мутации гена BRAF.
Согласно статистике, около 50% всех больных меланомой на поздних стадиях имеют мутацию этого гена. Её распространенность зависит от расположения опухоли:
- больные с меланомой на коже имеют мутацию более чем в 50% случаев;
- меланома слизистых оболочек содержит мутировавшие клетки в 5% случаев;
- меланома глаза никогда не сопровождается такой мутацией.
Когда применяется Дабрафениб?
Показания к применению препарата:
- метастазирующая меланома на поздних стадиях;
- неоперабельная меланома.
При применении Дабрафениба не назначаются другие виды лечения меланомы, такие как иммунотерапия, лучевая терапия, химиотерапия.
В 2012 году в журнале «Ланцет», — одном из самых авторитетных медицинских изданий, — были опубликованы результаты сравнения эффективности Дабрафениба и Дакарбазина — препарата, который наиболее часто используется для лечения меланомы. Выживаемость пациентов, принимавших Дабрафениб, оказалась существенно выше.
В 2014 году ученые опубликовали обновленные результаты исследования. В течение 2-х лет выживаемость пациентов, принимавших Дабрафениб, составила 45%, а тех, кто получал Дакарбазин — 32%.

Чаще всего при приеме Дабрафениба отмечаются такие побочные эффекты, как утолщение кожи (гиперкератоз), лихорадка, головная боль, боли в суставах, потеря слуха, папилломы кожи. Наиболее тяжелые возможные побочные эффекты, которые встречаются редко: падение артериального давления, тяжелые ознобы, обезвоживание, тяжелые нарушения функции почек, повышение уровня сахара крови. Перед назначением препарата всегда проводят исследование, которое помогает убедиться, что у больного имеется мутация гена BRAF. Широко применяется тест THxID BRAF Kit.
Европейская онкологическая клиника сотрудничает с израильскими, европейскими и американскими врачами, которые накопили значительный опыт в лечении иммунопрепаратами последнего поколения.
Иммунотерапия интерфероном при меланоме
Интерферон-альфа и интерлейкин-2 (ИЛ-2) — препараты, которые относятся к классу цитокинов, веществ, которые стимулируют иммунную систему. Их вводят внутривенно или под кожу. Цитокины могут быть назначены в двух случаях:
- При меланоме IV стадии. Интерферон и интерлейкин могут уменьшать размеры опухоли примерно на 10–20%. Их можно сочетать с химиопрепаратами.
- В качестве адъювантной терапии после операции. Цитокины применяют при меланомах, которые прорастают достаточно глубоко в кожу, в результате чего после хирургического лечения повышен риск рецидива. Интерферон-альфа и ИЛ-2 помогают предотвращать рецидивирование, но пока нет доказательств того, что они повышают выживаемость.
Во время лечения могут возникать такие побочные эффекты, как лихорадка, боли, озноб, депрессия, повышенная утомляемость. Иногда нарушаются функции печени и сердца.
Преимущества иммунотерапии при меланоме перед классической химиотерапией
Пожалуй, главное преимущество иммунотерапии перед «классической тройкой» лечения рака — химиотерапией, хирургией и лучевой терапией — в том, что она действует более физиологично. В то время как классические методы лечения нарушают и подавляют естественную иммунную защиту, иммунотерапия, напротив, активирует её.
Еще одно преимущество иммунотерапии в том, что она обладает так называемым «эффектом памяти». За счет этого лечебные эффекты в организме сохраняются в течение длительного времени после того, как завершен курс лечения. Это способствует повышению выживаемости.
Методы, которые применяются в иммунотерапии, в отличие от химиопрепаратов, не атакуют здоровые клетки. Благодаря этому побочных эффектов обычно меньше, они не такие серьезные. Как правило, с ними удается легче справиться с помощью поддерживающей терапии.
Наконец, иммунотерапия, открывает большие перспективы в лечении онкозаболеваний на будущее. Иммунитет человека, его взаимодействия с раковыми клетками — область науки, в которой остается большой простор для исследований, еще предстоит узнать много нового. Ученые и врачи не теряют надежду, что, возможно, в один прекрасный день это поможет кардинально изменить подходы к лечению рака, создать более эффективные методы и спасать больше жизней.
Отзывы об иммунотерапии при меланоме в Европейской клинике
Мне удаляли родинку в салоне. Это не первая родинка которую я удаляла, так что волноваться было вроде не о чем. А оказалось, что это меланома. Точнее не известно, была ли меланомой сама родинка, но эта процедура (криодеструкция) её как бы разбудила. В клинике, конечно, мне рассказали, какое «умное» решение я тогда приняла, но ничего не поделаешь. Хуже всего то, что самой отделённой родинки не осталось — она же была разрушена. Это на заметку хозяйкам, которые доверяют такие процедуры косметологам. Никогда так не делайте. Только больница. Там эту родинку отправят на исследование и скажут о ней всё. Так вот, лечить мне хотели химией. То есть не то, что хотели, а доктор сказала, что точно надо будет проводить химиотерапию. На всякий случай я обратилась в частную клинику, и там мне прямо с порога сказали, что никакой химиотерапии делать нельзя. Она работает только в 10% случаев, а ущерба для организма в десять раз больше чем пользы. Теперь есть препараты иммунотерапии. Это когда организм и сам может справиться, только ему надо помочь. Они есть ещё не во всех больницах, поэтому в предыдущей мне и назначали химию. Но это, что называется, по-старинке. А вот на иммунотерапию я согласилась и приняла решение лечиться здесь. И не зря, как видите. Чувствую себя прекрасно. Само лечение было не сказать чтобы тяжёлым — мне удалили участок кожи, с которого я удаляла родинку (сейчас под лопаткой просто очень светлое пятно с такой тонкой кожей на фоне моего многолетнего загара). А потом препарат. Результат, чтоб не сглазить, наилучший. По последним анализам, болезнь ушла. А вот загорать и кое-что есть мне всё ещё нельзя. Да уже как-то и не хочется, после таких приключений. Не думаю о том, что случилось бы, если бы не эти великие доктора. И никому не советую много думать — просто ищите решения и они найдутся.
Запись
на консультацию
круглосуточно
Источник