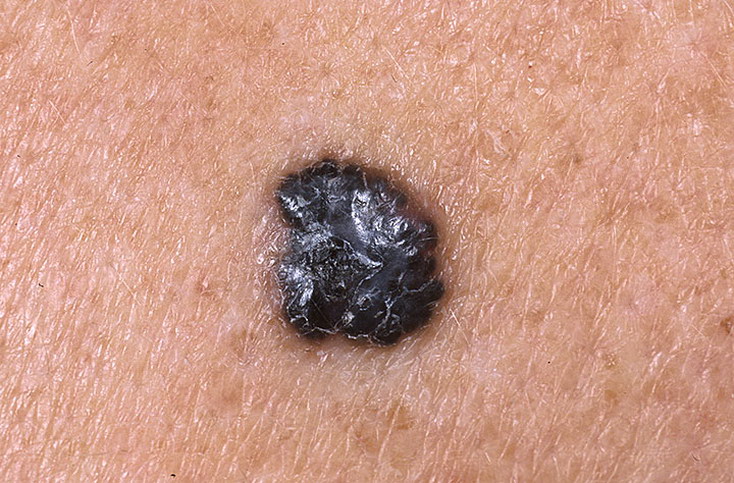
Генерализованные формы меланомы что это
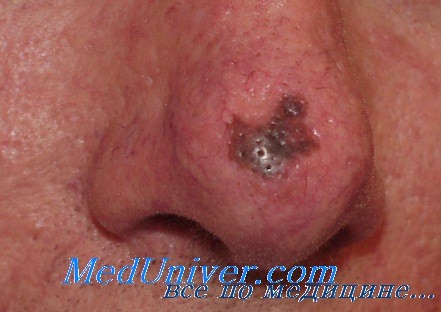
Меланома. Клиника и формы
• В 2013 г. в нашей стране было зарегистрировано примерно 59940 случаев инвазивной меланомы кожи и дополнительно 48290 случаев меланомы in situ.
• В 2013 г. в нашей стране от метастазирующей меланомы умерло примерно 8110 человек.
• Хотя в 1970-х годах заболеваемость меланомой в нашей стране возросла, с 1990 гг. уровень заболеваемости стабилизировался.
• В одном из исследований было показано, что за пятилетний период заболеваемость меланомой возросла в 2,4 раза, в то время как число биопсий за тот же период также увеличилось в 2,5 раза. Эти данные свидетельствуют не о росте заболеваемости меланомой, а о повышении частоты выявления опухоли.
• Средний возраст пациентов при первичном выявлении меланомы составляет 53 года.
• Меланома является самым распространенным видом рака у женщин в возрасте от 25 до 29 лет.
Факторы риска меланомы
Существует связь между солнечным ожогом в раннем возрасте и риском развития меланомы.
К первичным факторам риска возникновения меланомы относятся:
– Изменение вида родинки (самый важный фактор риска).
– Атипичные/диспластические невусы (особенно более 5-10).
– Большое количество обычных невусов (более 100).
– Большие (гигантские) врожденные невусы (диаметром более 20 см у взрослых).
– Анамнез.
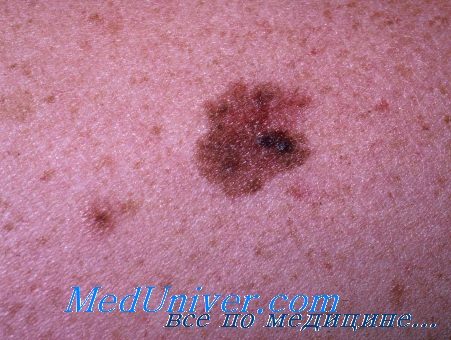
– Чувствительность к солнечному излучению/избыточное пребывание на солнце или солнечные ожоги.
– Меланома у родственника первой линии родства.
– Немеланомный рак кожи (базальноклеточная или плоскоклеточная карцинома).
– Мужской пол.
– Возраст старше 50 лет.
– Наличие пигментной ксеродермы или синдрома семейных атипичных невусов и меланомы.
– Светлый фенотип кожи (голубые/зеленые глаза, белокурые/рыжие волосы, светлый цвет лица, чувствительность к солнечному излучению) и солнечный ожог с пузырями в детском и подростковом возрасте.
Диагностика меланомы
Для диагностики меланомы применяется мнемоническое правило ABCDE:
А = Assymetry (асимметрия). Большинство ранних очагов меланомы ассиметричны: линия, проведенная через центр очага, не делит образование на одинаковые половины. Доброкачественные невусы обычно округлые и симметричные.
В = Border (граница). Границы ранних очагов меланомы часто неровные, образования могут иметь фестончатые или зазубренные края. У доброкачественных невусов края очага более гладкие, границы более ровные.
С = Color (цвет). Неравномерность цветовой окраски. Доброкачественные невусы обычно окрашены в один оттенок коричневого цвета, у меланомы часто наблюдается неравномерная пигментация: различные оттенки коричневого, желто-коричневого или черного цвета. По мере развития меланомы могут становиться красными, белыми и синеватыми.

D = Diameter (диаметр). Диаметр очага обычно более или равен 6 мм. Ранние очаги меланомы обычно более крупные, чем большинство невусов (помните, что врожденные невусы нередко бывают крупными).
E = Evolving (эволюция или динамика развития). Любой растущий или изменяющийся очаг должен вызывать подозрение на меланому. Динамические изменения могут затрагивать размер, форму, симптомы (зуд, болезненность), состояние поверхности (особенно кровоточивость) и пигментацию.
• В проспективном контролируемом исследовании при сравнении 460 случаев меланомы и 680 случаев доброкачественных пигментированных опухолей были выявлены значительные расхождения по каждому из критериев ABCDE между меланомами и доброкачественными невусами.
• Чувствительность критериев составила: А – 57%, 15 – 57%, С – 65%, D – 90%, Е – 84%. Специфичность: А – 72%, В -I %, С – 59%, D – 63%, Е – 90%.
• Чувствительность критериев ABCDE изменяется в зависимости от их количества: при оценке двух критериев она достигает 89,3%, трех- 65,5%; специфичное и для двух критериев составляла 65,3%, при трех – 81 %.
• Число положительных критериев было различным при доброкачественных невусах (1,24±1,26) и ме-ланомах (3,53±1,53). К сожалению, статистически значимой разницы между мелапомами и атипичными невусами не обнаружено.

Существует четыре основные формы меланомы. За исключением узловой меланомы, для остальных трех форм характерна фаза радиального роста, при которой отсутствует потенциал метастазирования и которая до инвазии в дерму может длиться от нескольких месяцев до нескольких лет. Ниже описаны основные формы меланом:
1. Поверхностно распространяющаяся меланома – самая распространенная форма опухоли, регистрируемая В 70% случаев всех меланом. До инвазии в дерму для этой формы характерен радиальный рост. Первым признаком заболевания является появление плоского пятна или слегка выступа ющей над поверхностью бляшки необычного цвета с неровными краями и близкой к правильной форме. Цвет очагов различный: отмечаются участки желто коричневого, коричневого, черного, красного, синего или белого цвета. Такие очаги нередко появляются на месте невуса. Меланома может возникать на любом участке тела, но у мужчин она чаще всего встречается на туловище, у женщин – на ногах, а на верхней части спины меланома наблюдается у обоих полов. Большинство меланом, обнаруженных у молодых людей, представляет собой поверхностно распространяющуюся форму опухоли.
2. Узловая меланома встречается в 15-30% случаев. На момент установления диагноза она обычно инвазивная, ее злокачественный характер распознается по выступающему узлу. Цвет чаще всего черный, но иногда отмечается синий, серый, белый, коричневый, смугло-желтый, красный цвет, либо его полное отсутствовие.
3. Лентиго-меланома наблюдается в 4-15% случаев кожных меланом. Она похожа на поверхностно распространяющуюся меланому и выглядит как плоский или слегка выступающий над поверхностью пятнистый, светло-коричневый, коричневый или темно-коричневый очаг пигментации кожи. Такая форма меланомы чаще всего выявляется у пожилых людей. Она развивается на участках, постоянно подверженных воздействию солнечного излучения: па поврежденной коже лица, ушных раковин, рук и верхней части туловища. Средний возраст начала заболевания составляет 65 лет, опухоль медленно растет в течение 5-20 лет. Злокачественное лентиго трансформируется в меланому примерно в 5% случаев. Этот предраковый очаг in situ обычно более 3 мм в диаметре и существует до трансформации не менее 10-15 лет.
4. Акральная лентигинозная меланома – наиболее редкая форма меланомы (2-8% случаев меланомы у лиц с белой кожей; 29-72% случаев мелапомы у лиц с темной кожей). Она развивается под ногтевой пластинкой, на ладонях или подошвах. Из-за позднего установления диагноза эта форма связана с худшим прогнозом. Подногтевая меланома может проявляться как диффузное изменение окраски ногтя или продольная пигментированная полоска в пределах ногтевой пластинки. Когда подногтевой пигмент распространяется на проксимальный или латеральный ногтевой валик, возникает так называемый симптом Гетчинсона, с большой вероятностью указывающий на акральную лентигинозную меланому.
К более редким формам меланомы относятся:
• Амеланотическая меланома (менее 5% случаев всех меланом) лишена пигментации и представляет собой очаг розового или телесного цвета, часто имитирующий базальноклеточпую/плоскоклеточную карциному, или разрушенный волосяной фолликул. Амеланотическая меланома является либо разновидностью узловой меланомы, либо метастазом меланомы в кожу и развивается в результате неспособности мало-дифферепцированных раковых клеток синтезировать меланиновый пигмент.
• Другие редкие варианты меланомы включают:
1) десмопластическую/нейротропную меланому,
2) (лентигинозную) меланому слизистых оболочек,
3) злокачественный голубой иевус и
4) меланому, разни вающуюся в гигантском врожденном невусе.
Наиболее часто меланома встречается на туловище у белокожих мужчин и на голенях и спине у белокожих женщин. У лиц афроамериканского, азиатского и латиноамериканского происхождения самой распространенной локализацией меланомы являются подошвенная поверхность, подногтевая область, ладонная поверхность и слизистые оболочки.
– Также рекомендуем “Инструментальная диагностика меланомы. Дифференциация”
Оглавление темы “Поражения кожи”:
- Кожный рог. Диагностика и лечение
- Базальноклеточная карцинома. Причина и диагностика
- Лечение базальноклеточной карциномы. Рекомендации
- Плоскоклеточная карцинома. Причины появления и диагностика
- Лечение плоскоклеточной карциномы. Рекомендации
- Меланома. Клиника и формы
- Инструментальная диагностика меланомы. Дифференциация
- Лечение меланомы. Рекомендации
- Кольцевидная гранулема. Причина появления и диагностика
- Лечение кольцевидной гранулемы. Рекомендации
Источник
Изобретение относится к медицине, в частности к онкологии, и касается лечения генерализованной меланомы кожи. Для этого из подвздошной кости больного получают костно-мозговую взвесь и центрифугируют ее 30 мин при 2200 об/мин. Форменные элементы костно-мозговой взвеси инкубируют с химиопрепаратами в термостате при 37°С в течение 30 мин. Затем осуществляют их реинфузию больному внутривенно капельно 1 раз в неделю. Плазму каждый раз отбирают и замораживают при -40°С. Выполняют пять таких процедур. Затем показаниям проводят лучевое лечение. Через две недели после окончания лучевой терапии порционно размораживают плазму костно-мозговой взвеси. После инкубации с химиопрепаратами в термостате при 37°С в течение 30 мин и плазму реинфузируют больному внутривенно капельно 1 раз в неделю. Выполняют пять таких процедур. Способ обеспечивает возможность воздействия на метастазы меланомы химиотерапии в высоких дозах с достижением их стабилизации или полной резобции без проявлений токсичности III-IV степени.
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для лечения больных меланомой кожи, которым противопоказано оперативное лечение.
Несмотря на достигнутые успехи в области медикаментозного лечения онкологических больных, диссеминированная или генерализованная форма меланомы кожи по-прежнему считается практически инкурабельным заболеванием.
Известно что основным методом лечения при генерализованных формах меланомы является лекарственный (“Противоопухолевая химиотерапия” под ред. Н.Н.Переводчиковой, М.: Медицина, 1993, с.41-43) путем введения различных химиопрепаратов и их сочетаний. Препаратами, эффективность которых составляет 20% и немногим более, является дакарбазин, производные платины. Циклофосфан, прокарбозин, винбластин, CCNU, дактиномицин, виндезин, гидроксимочевина эффективны у 10-20% больных.
Большинство алкилирующих агентов и антиметаболитов эффективны менее чем у 10% больных. Кожные метастазы меланомы и в лимфатические узлы более чувствительны к лекарственной терапии по сравнению с метастазами в легкие. Метастазы в печень, кости, головной мозг практически нечувствительны к химиотерапии. Лучшим препаратом при генерализованной меланоме кожи считают дакарбазин, который применяется как препарат первой линии, его эффективность составляет 20-25%. Однако добиться полной регрессии при его использовании, как правило, вообще не удается. Ремиссия при этом продолжается в среднем 4-6 месяцев.
Известно что при выборе лечебного воздействия необходимо руководствоваться локализацией метастатического поражения. При наличии метастазов в головной мозг, которые выявляются клинически у 8-46% больных с генерализованной меланомой кожи, преимущества имеют производные нитрозомочевины, поскольку препараты этой группы способны проникать через гематоэнцефалический барьер (Delaunay M., Mohr P., Momex F. et al. A randomized phase III trial of fotemustine versus fotemustine combined with wohle brain radiation for braian metastases of melanoma. Ninth international congress on anti-cancer treatment, 1999. – Abstr. 96). Авторы применяли фотемустин по 100 мг/м2 в 1-й и 8-й дни на фоне лучевой терапии у 76 больных меланомой кожи с метастазами в головной мозг.
Однако эффективность при таком методе лечения составила 7% и 10% соответственно после приема одного фотемустина и в сочетании его с лучевой терапией, а медиана выживаемости – 85 дней и 105 дней соответственно (Р>0,05).
Известен способ лечения генерализованной меланомы (Meisen-berg B.R., Ross M., Vredenburg J.J. et al. Randomized trial of high-dose chemotherapy with autologus bone marrow suport as adjuvant therapy for high-risk, multi-node-positive malignant melanoma // J. Nat. Cancer Inst. – 1993. – V.16, Suppl.1. – P.34-44). Авторы изучали эффективность высокодозной химиотерапии в сочетании с аутологичной трансплантацией костного мозга при меланоме кожи с множественным метастатическим поражением регионарных лимфатических узлов. В исследование были включены 39 пациентов с метастазами в 5 и более лимфатических узлах. 19 больных в течение 4 дней получали высокодозную химиотерапию циклофосфаном в дозе 5625 мг/м2, цисплатином в дозе 165 мг/м2, BCNU в дозе 600 мг/м2. Через 3 дня после химиотерапии выполнялась реинфузия аутологичного костного мозга. Группа контроля состояла из 20 пациентов, находившихся под наблюдением до возникновения рецидива заболевания.
Однако отмечена чрезвычайно плохая переносимость и выраженная токсичность высокодозного режима введения: более чем у 2/3 больных имелись проявления токсичности III и IV степени выраженности, а медиана безрецидивного периода в группе, получавшей химиотерапию с аутотрансплантацией костного мозга составила 35 недель, против 16 в контроле. Различий в общей выживаемости не получено.
Целью настоящего изобретения является улучшение результатов консервативного лечения больных с генерализованной меланомы кожи.
Поставленная цель достигалась тем, что больным проводят пункцию подвздошной кости, забирают 180-200 мл костно-мозговой взвеси, центрифугируют ее, отбирают клеточную массу, которую инкубируют с химиопрепаратами: цисплатин – 100 мг/м2, метотрексат – 25 мг/м2, циклофосфан – 1000 мг/м2, а плазму костно-мозговой взвеси замораживают при -40°С и хранят в морозильной камере. Такую процедуру повторяют 1 раз в неделю в течение 5 недель, каждый раз замораживая плазму костно-мозговой взвеси. Затем больного подвергают лучевому лечению стандартными методиками по показаниям. Через 2 недели после лучевого лечения на порциях размороженной плазмы костно-мозговой взвеси проводят химиотерапию 500 мг/м2 дакарбозином 1 раз в неделю.
Изобретение является новым, так как оно неизвестно из уровня медицины в области онкологии при лечении генерализованной формы меланомы кожи химиотерапевтическими средствами в сочетании с лучевой терапией. Новизна изобретения заключается в том, что при лечении генерализованной формы меланомы кожи химиопрепараты вводят на клеточных элементах костно-мозговой взвеси больного, осуществляют лучевое лечение, а затем проводят химиотерапию на размороженной плазме костно-мозговой взвеси больного. Изобретение имеет изобретательский уровень, так как оно не известно для специалиста-онколога в этой области, и явным образом не следует из уровня клинической онкологии.
В доступных источниках информации России, стран СНГ и за рубежом указаний на подобный способ улучшения результатов лечения генерализованной формы меланомы кожи не обнаружено.
Изобретение является промышленно применимым, так как может быть многократно воспроизведено и применено в здравоохранении, в лечебных учреждениях специализированного профиля.
Способ осуществляется следующим образом. Больным генерализованной формы меланомы кожи проводят пункцию тазовых костей, собирают костно-мозговую взвесь, центрифугируют ее в течение 30 мин при 2200 об/мин. Затем плазму костно-мозговой взвеси замораживают при температуре -40°С с последующим хранением при -18°С. Клеточную массу костно-мозговой взвеси инкубируют с цитостатиками: цисплатин – 100 мг/м2, метотрексата – 25 мг/м2, циклофосфан – 1000 мг/м2 в термостате в течение 30 мин, при температуре 37°С, а затем вводят пациенту внутривенно капельно.
Перед введением цисплатина проводят регидратацию в стандартном объеме. Всего проводят 5 аналогичных курсов фракционной аутомиелохимиотерапии 1 раз в неделю, вводя химиопрапараты после их инкубации с клеточной массой костно-мозговой взвеси, а плазму замораживая. Через две недели после последнего введения химиопрепаратов на клеточной массе костно-мозговой взвеси больным проводят курс лучевой терапии в стандартном режиме по показаниям. Через 2 недели после лучевого лечения проводят повторные курсы химиотерапии. Для этого плазму костно-мозговой взвеси порционно размораживают, 500 мг/м2 дакарбазина инкубируют с размороженной плазмой костно-мозговой взвеси в термостате в течение 30 мин, при температуре 37°С, а затем вводят пациенту внутривенно капельно.
Для доказательства приводим выписку из историй болезни, подтверждающую клинический эффект лечения предлагаемым способом.
Пример. Больной К., 1959 года рождения (ист. бол. №12654/л) находится под наблюдением РНИОИ с 28.01.02 с диагнозом меланома кожи надключичной области справа pT2N0M0. Состояние после комбинированного лечения (2001 г.). Генерализация процесса.
Из анамнеза. В октябре 2001 года проведена дистанционная гамматерапия на пигментное образование в правой надключичной области и зону регионарного метастазирования (шейно-над-подключичные лимфатические узлы) в суммарной очаговой дозе 40 Гр. 12.10.01 осуществлено оперативное иссечение первичного опухолевого очага. Гистоисследование №25311-25313 от 12.10.01 – веретеноклеточная меланома, III уровень инвазии по Кларку, толщина опухоли по Бреслоу 12 мм. На основании проведенного обследования выписан с клиническим выздоровлением.
В январе 2002 года жалобы на появление в зоне послеоперационного рубца пигментного узелка размерами 0,4 см плотного с бугристыми краями. Сухой кашель, тяжесть и боли в грудной клетке.
Обследован. ФЛО №36 от 30.01.02 – солитарный метастаз в корень правого легкого. При СРКТ «метастаз в корень правого легкого диаметром до 2,8 см, увеличенные перибронхиальные и паратрахеальные лимфоузлы справа, вероятнее всего, метастатического характера
УЗИ от 30.01.02 периферические лимфоузлы не увеличены, печень без очаговых образований. Цитологическая верификация образования на коже правой надключичной области №208/02 – метастаз меланомы. OAK от 31.01.02 Hb – 128 г/л; Эр. – 4,0×1012/л; Л – 7,2×109%; баз -1%; эозин. – 1%; пал. – 8%; сегм. – 59%; лимф. – 28%; мон. – 3%. СОЭ – 25 мм/ч.
04.02.02 под местным обезболиванием произведена трепанопункция левой подвздошной кости с эксфузией 200 мл костно-мозговой взвеси (КМВ). Осуществлено центрифугированние КМВ в течение 30 минут при 2200 об/мин. Плазма КМВ заморожена при температуре -40°С и отправлена на хранение при температуре -18°С.
Клеточная масса аутомиеловзвеси после предварительной инкубации в течение 30 минут при t 37°C, со 100 мг цисплатина введена внутривенно на фоне гипергидратации. На физиологическом растворе введены метотрексат 25 мг и циклофосфана 1000 мг.
Указанные манипуляции осуществлены данному пациенту с интервалом 1 раз в неделю – 04.02.02; 11.02.02; 18.02.02; 25.02.02 и 04.03.02.
С 11.03.02 по 05.04.02 проведен курс дистанционной гамматерапии на область средостения с включением коря правого легкого. Облучение выполнялось дробно-протяженно в режиме стандартного фракционирования с ежедневным подведением разовой очаговой дозы 2 Гр с трех полей размерами 6×15 см, под углами 0°, 75°, 285°. Суммарная очаговая доза составила 40 Гр за 20 фракций. Курс облучения без осложнений. OAK от 05.04.02 Hb – 118 г/л; Эр. – 3,5×1012/л; Л – 3,2×109/л; баз – 0%; эозин. – 1%; пал. – 3%; сегм. – 73%; лимф. – 18%; мон. – 5%. СОЭ – 15 мм/ч.
После двухнедельного перерыва 22.04.02; 29.04.02; 07.05.02; 15.05.02; 22.05.02 и 31.05.02 проведены 5 курсов химиотерапии.
Для этого плазму костно-мозговой взвеси порционно размораживали, инкубировали ее в течение 30 минут при t 37°C с 750 мг дакарбазина и вводили внутривенно капельно.
Общая доза цитостатиков за весь курс аутомиелополихимиотерапии составил: цисплатина – 500 мг; циклофосфана – 5000 мг; метотрексата – 125 мг и дакарбазина – 3750 мг.
При контрольном исследовании 03.06.02 ФЛО №19351 полная регрессия метастатического компонента в корнях легких. При СРКТ – в корне правого легкого и средостении без патологических образований. Также отмечена полная регрессия кожного сателлита в правой надключичной области.
OAK от 03.06.02 Hb – 108 г/л; Эр. – 3,6×1012/л; Л – 3,5×109/л; баз – 0%; эозин. – 1%; пал. – 6%; сегм. – 67%; лимф. – 16%; мон. – 5%. СОЭ – 12 мм/ч.
Больной наблюдается в течение 30 месяцев (последняя явка и контрольное обследование) без признаков локальных рецидивов и регионарных или отдаленных метастазов.
Указанным способом было пролечено 30 больных генерализованной формой меланомы кожи: 10 из которых имели метастазы в легкие, 8 – в мозг, 12 – в мягкие ткани. После проведенного лечения у 6 больных имелись рентгенологические признаки полной регрессии метастазов в легкие, у 4 – стабилизация метастатического процесса в легких. Медиана выживаемости в этой группе пациентов составила 20 мес. У 2 больных имелись рентгенологические признаки полной регрессии метастазов в мозг, у 6 пациентов – рентгенологическое уменьшение метастатических очагов в мозге на 25-50%. Медиана выживаемости в этой группе пациентов составила 14 мес. У 10 пациентов произошла полная резорбция метастазов в мягкие ткани, у 2 – уменьшение процесса более чем на 50%. Медиана выживаемости в этой группе пациентов составила 24 мес. Ни в одном случае при применении указанного способа не было токсичности III и IV степени.
Техническо-экономический эффект от использования “Способа лечения генерализованной меланомы кожи” заключается в возможности улучшить результаты и качество жизни больных; уменьшить патологические побочные проявления противоопухолевой терапии.
Способ лечения генерализованной меланомы кожи, включающий введение химиопрепаратов на аутосредах и лучевую терапию, отличающийся тем, что взятую из подвздошной кости больного костно-мозговую взвесь центрифугируют 30 мин при 2200 об/мин, плазму отбирают и замораживают при -40°С, форменные элементы костно-мозговой взвеси инкубируют с химиопрепаратами в термостате при 37°С в течение 30 мин и реинфузируют больному внутривенно капельно, проводя 5 таких процедур 1 раз в неделю, каждый раз замораживая плазму костно-мозговой взвеси, далее по показаниям проводят лучевое лечение, после которого через 2 недели порционно размораживают плазму костно-мозговой взвеси, инкубируют ее с химиопрепаратами в термостате при 37°С в течение 30 мин и реинфузируют больному внутривенно капельно, проводя 5 таких процедур 1 раз в неделю.
Источник