Впч количественное в инвитро

Метод определения
ПЦР.
Исследуемый материал
Соскоб эпителиальных клеток урогенитальный
Тест, направленный на раздельное качественное обнаружение вируса папилломы человека 14 типов высокого онкогенного риска: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 в соскобе эпителиальных клеток урогенитального тракта.
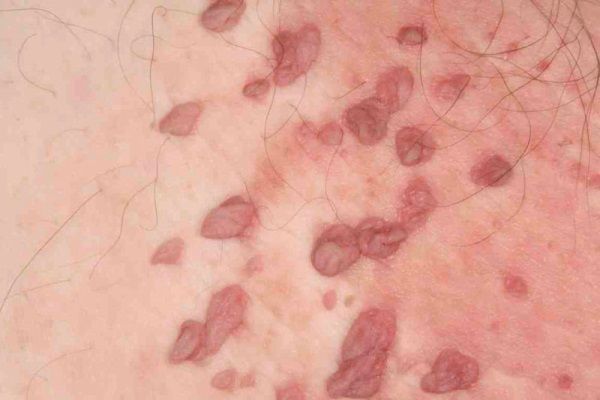
Вирус папилломы человека (ВПЧ) может быть причиной возникновения рака гениталий у женщин и плоскоклеточного рака у мужчин и женщин. Доказано, что этот вирус является причиной возникновения остроконечных кондилом, кондилом и новообразований шейки матки. Различные виды ВПЧ являются причиной различных поражений. Некоторые из них являются факторами высокого онкогенного риска.
Необходимым условием получения достоверного результата исследования является соблюдение техники взятия соскоба эпителиальных клеток. В состав тестов по диагностике и мониторингу ВПЧ введен специальный параметр – контроль взятия материала (КВМ). КВМ представляет собой тест по определению количества геномной ДНК человека в биоматериале, источником которой являются эпителиальные клетки, попадающие в пробу при правильной технике взятия биоматериала.
Аналитические показатели.
- определяемый фрагмент – специфичные участки ДНК ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 типов;
- специфичность определения – 100%;
- чувствительность определения 100 копий ДНК ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 типов в образце.
Литература
- Профилактика рака шейки матки: Руководство для врачей. – М.: МЕДпресс-информ, 2008.
- Полонская Н.Ю., Юрасова И.В., Сокольская Т.Ю. Преимущества и эффективность стандвртизации цитологических исследований в гинекологии // Клиническая лабораторная диагностика. – 2004. №11 с.47-50.
- Bekkers R., Meijer C., et al. Effects of HPV detection in population-based screening programmers for cervical cancer: a Dutch moment // Gynecol. Oncol. 2006; Mar: 100(3):451-4.
- Khan M., et al. The elevated 10-year risk of cervical precancer and cancer in women with human papillomavirus (HPV) type 16 or 18 and the possible utility of type specific HPV testing in clinical practice // J. nat. cancer inst. 2005; 97:1072-9.
- Snijders J., Meijer C. The value of viral load in HPV detection in screening // HPV today 2006; 8:8-9.
Обследование женщин целесообразно проводить в первую половину менструального цикла, не ранее 5 –ого дня. Допустимо обследование во второй половине цикла, не позднее, чем за 5 дней до предполагаемого начала менструации. При наличии патологических изменений, взятие материала проводится в день обращения. Накануне и в день обследования пациентке не рекомендуется выполнять спринцевание влагалища. Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии (общей / местной) и во время menses, ранее 24- 48 часов после полового контакта, интравагинального УЗИ и кольпоскопии. Рекомендуется брать материал не ранее, чем через 14 дней после применения антибактериальных препаратов и местных антисептиков, и не ранее, чем через 1 месяц после применения антибиотиков перорально. Если для исследования берут соскоб из уретры, сбор материала проводят до или не ранее 2 – 3 часов после мочеиспускания.
Для мужчин: За 1–2 суток до взятия мазка (соскоба) необходимо исключить половые контакты. Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии (общей / местной). Нельзя мочиться в течение 1,5-2 часов до процедуры.
С общими рекомендациями для подготовки к исследованиям можно ознакомиться
здесь >>
Проявления трансформирующей дисплазии в различной степени.
Ослабление иммунитета.
Профилактические скрининговые исследования.
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Тест качественный. Формат выдачи результата включает ответ по каждому из указанных типов ВПЧ – ОБНАРУЖЕНО/НЕ ОБНАРУЖЕНО.
Контроль взятия материала:
Тест КВМ выполняется до проведения тестов по выявлению ДНК ВПЧ. В случае, если в пробе значение КВМ неудовлетворительное, т.е. менее 4 lg (10000) копий ДНК человека в пробе, исследование ДНК ВПЧ не проводится и рекомендуется повторное взятие биологического материала.
Обращаем внимание, что сроки выполнения ПЦР-исследований могут быть увеличены при проведении подтверждающих тестов.
Артикул:
313С-УРО
Срок исполнения:
до 2 рабочих дней ?
Указанный срок не включает день взятия биоматериала
Цена:
1 080 руб
Взятие мазка/соскоба:
- + 400 руб
В этом разделе вы можете узнать, сколько стоит выполнение данного исследования в вашем городе, ознакомиться с описанием теста и таблицей интерпретации результатов. Выбирая, где сдать анализ «Дифференцированное определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) высокого онкогенного риска 14 типов (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) + КВМ в соскобе эпителиальных клеток урогенитального тракта» в Москве и других городах России, не забывайте, что цена анализа, стоимость процедуры взятия биоматериала, методы и сроки выполнения исследований в региональных медицинских офисах могут отличаться.
Источник
Метод определения
ПЦР с детекцией в режиме «реального времени».
Исследуемый материал
Соскоб эпителиальных клеток урогенитальный
Определение ДНК вируса папилломы человека (ВПЧ) 16, 18 типа (HPV 16, 18) в соскобе эпителиальных клеток урогенитального тракта методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени».
Вирус папилломы человека (ВПЧ) может быть причиной возникновения рака гениталий у женщин и плоскоклеточного рака у мужчин и женщин. Доказано, что этот вирус является причиной возникновения остроконечных кондилом, кондилом и новообразований шейки матки. Различные виды ВПЧ являются причиной различных поражений. Некоторые из них являются факторами высокого онкогенного риска. Более 90% всех цервикальных карцином позитивны к присутствию ВПЧ. Наиболее часто в материале из опухолей шейки матки обнаруживаются 16 и 18 типы ВПЧ. Обнаружение в исследуемом материале ВПЧ не говорит о наличии злокачественного процесса, но требует дополнительного гистологического исследования и динамического наблюдения.
Необходимым условием получения достоверного результата исследования является соблюдение техники взятия соскоба эпителиальных клеток. В состав тестов по диагностике и мониторингу ВПЧ введен специальный параметр – контроль взятия материала (КВМ). КВМ представляет собой тест по определению количества геномной ДНК человека в биоматериале, источником которой являются эпителиальные клетки, попадающие в пробу при правильной технике взятия биоматериала.
Аналитические показатели:
- определяемый фрагмент – специфичные участки ДНК ВПЧ 16, 18 типа;
- специфичность определения – 100%;
- чувствительность определения 100 копий ДНК ВПЧ 16, 18 типа в образце.
Литература
- Профилактика рака шейки матки: Руководство для врачей. – М.: МЕДпресс-информ, 2008.
- Полонская Н.Ю., Юрасова И.В., Сокольская Т.Ю. Преимущества и эффективность стандвртизации цитологических исследований в гинекологии // Клиническая лабораторная диагностика. – 2004. №11 с.47-50.
- Bekkers R., Meijer C., et al. Effects of HPV detection in population-based screening programmers for cervical cancer: a Dutch moment // Gynecol. Oncol. 2006; Mar: 100(3):451-4.
- Khan M., et al. The elevated 10-year risk of cervical precancer and cancer in women with human papillomavirus (HPV) type 16 or 18 and the possible utility of type specific HPV testing in clinical practice // J. nat. cancer inst. 2005; 97:1072-9.
- Snijders J., Meijer C. The value of viral load in HPV detection in screening // HPV today 2006; 8:8-9.
Обследование женщин целесообразно проводить в первую половину менструального цикла, не ранее 5 –ого дня. Допустимо обследование во второй половине цикла, не позднее, чем за 5 дней до предполагаемого начала менструации. При наличии патологических изменений, взятие материала проводится в день обращения. Накануне и в день обследования пациентке не рекомендуется выполнять спринцевание влагалища. Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии ( общей / местной) и во время menses, ранее 24- 48 часов после полового контакта, интравагинального УЗИ и кольпоскопии. Рекомендуется брать материал не ранее, чем через 14 дней после применения антибактериальных препаратов и местных антисептиков, и не ранее, чем через 1 месяц после применения антибиотиков перорально. Если для исследования берут соскоб из уретры, сбор материала проводят до или не ранее 2 – 3 часов после мочеиспускания.
Для мужчин: За 1–2 суток до взятия мазка (соскоба) необходимо исключить половые контакты. Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии ( общей / местной). Нельзя мочиться в течение 1,5-2 часов до процедуры.
С общими рекомендациями для подготовки к исследованиям можно ознакомиться
здесь >>
Проявления трансформирующей дисплазии в различной степени.
Ослабление иммунитета.
Профилактические скрининговые исследования.
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Тест качественный. Результат выдаётся в терминах «обнаружено» или «не обнаружено» для каждого типа ВПЧ (16, 18).
- «обнаружено»: в анализируемом образце биологического материала найдены фрагменты ДНК, специфичные для ВПЧ 16, 18 типа; инфицирование ВПЧ указанного типа.
- «не обнаружено»: в анализируемом образце биологического материала не найдено фрагментов ДНК, специфичных для ВПЧ 16, 18 типа или концентрация возбудителей в образце ниже границы чувствительности теста.
Контроль взятия материала:
Тест КВМ выполняется до проведения тестов по выявлению ДНК ВПЧ. В случае, если в пробе значение КВМ неудовлетворительное, т.е. менее 4 lg (10000) копий ДНК человека в пробе, исследование ДНК ВПЧ не проводится и рекомендуется повторное взятие биологического материала.
Обращаем внимание, что сроки выполнения ПЦР-исследований могут быть увеличены при проведении подтверждающих тестов.
Источник
Метод определения
ПЦР.
Исследуемый материал
Соскоб эпителиальных клеток ротоглотки
Тест, направленный на качественное обнаружение ДНК вируса папилломы человека 14 типов высокого онкогенного риска: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 в соскобе эпителиальных клеток урогенитального тракта.
Вирус папилломы человека (ВПЧ) может быть причиной возникновения рака гениталий у женщин и плоскоклеточного рака у мужчин и женщин. Доказано, что этот вирус является причиной возникновения остроконечных кондилом, кондилом и новообразований шейки матки. Различные виды ВПЧ являются причиной различных поражений. Некоторые из них являются факторами высокого онкогенного риска.
Необходимым условием получения достоверного результата исследования является соблюдение техники взятия соскоба эпителиальных клеток. В состав тестов по диагностике и мониторингу ВПЧ введен специальный параметр – контроль взятия материала (КВМ). КВМ представляет собой тест по определению количества геномной ДНК человека в биоматериале, источником которой являются эпителиальные клетки, попадающие в пробу при правильной технике взятия биоматериала.
Аналитические показатели:
- определяемый фрагмент – специфичные участки ДНК ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 типов;
- специфичность определения – 100%;
- чувствительность определения 100 копий ДНК ВПЧ 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 типов в образце.
Литература
- Профилактика рака шейки матки: Руководство для врачей. – М.: МЕДпресс-информ, 2008.
- Полонская Н.Ю., Юрасова И.В., Сокольская Т.Ю. Преимущества и эффективность стандвртизации цитологических исследований в гинекологии // Клиническая лабораторная диагностика. – 2004. №11 с.47-50.
- Bekkers R., Meijer C., et al. Effects of HPV detection in population-based screening programmers for cervical cancer: a Dutch moment // Gynecol. Oncol. 2006; Mar: 100(3):451-4.
- Khan M., et al. The elevated 10-year risk of cervical precancer and cancer in women with human papillomavirus (HPV) type 16 or 18 and the possible utility of type specific HPV testing in clinical practice // J. nat. cancer inst. 2005; 97:1072-9.
- Snijders J., Meijer C. The value of viral load in HPV detection in screening // HPV today 2006; 8:8-9.
Взятие материала желательно проводить до диагностических и лечебных манипуляций в предполагаемом месте локализации возбудителя.
Взятие биологического материала рекомендуется проводить до начала применения лекарственных препаратов (антибактериальных, противовирусных, противопаразитарных). При проведении исследований в целях контроля лечения целесообразно проводить взятие проб на ПЦР-тесты не ранее, чем через 10-14 дней после окончания применения соответствующих препаратов локального действия и не ранее, чем через один месяц после проведения системной терапии.
При подготовке пациента к процедуре следует учесть:
- за 6 часов до исследования не рекомендуется использовать лекарственные средства для орошения ротоглотки и препараты для рассасывания;
- перед проведением исследования не чистить зубы, не использовать жевательную резинку/пастилки для освежения дыхания;
- перед началом исследования прополоскать полость рта водой комнатной температуры.
Желательно соблюдать все описанные условия, если лечащим врачом не рекомендовано иное.
Проявления трансформирующей дисплазии в различной степени.
Ослабление иммунитета.
Профилактические скрининговые исследования.
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Формат выдачи результата включает суммарный ответ по всем указанным типам ВПЧ-обнаружено/не обнаружено. Результат ОБНАРУЖЕНО следует интерпретировать как наличие в образце специфических участков ДНК одного или нескольких типов ВПЧ без указания конкретного типа. Результат НЕ ОБНАРУЖЕНО следует интерпретировать как отсутствие в образце специфических участков ДНК ВПЧ всех указанных типов.
Контроль взятия материала:
Тест КВМ выполняется до проведения тестов по выявлению ДНК ВПЧ. В случае, если в пробе значение КВМ неудовлетворительное, т.е. менее 4 lg (10000) копий ДНК человека в пробе, исследование ДНК ВПЧ не проводится и рекомендуется повторное взятие биологического материала.
Обращаем внимание, что сроки выполнения ПЦР-исследований могут быть увеличены при проведении подтверждающих тестов.
Артикул:
311С-РОТ
Срок исполнения:
до 2 рабочих дней ?
Указанный срок не включает день взятия биоматериала
Цена:
910 руб
Взятие мазка/соскоба:
- + 400 руб
В этом разделе вы можете узнать, сколько стоит выполнение данного исследования в вашем городе, ознакомиться с описанием теста и таблицей интерпретации результатов. Выбирая, где сдать анализ «Определение ДНК ВПЧ (Вирус папилломы человека, Human papillomavirus, HPV) высокого онкогенного риска, скрининг 14 типов (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68) + КВМ в соскобе эпителиальных клеток ротоглотки» в Москве и других городах России, не забывайте, что цена анализа, стоимость процедуры взятия биоматериала, методы и сроки выполнения исследований в региональных медицинских офисах могут отличаться.
Источник
Метод определения
ПЦР с детекцией в режиме «реального времени».
Исследуемый материал
Соскоб эпителиальных клеток урогенитального тракта
Количественное определение ДНК ВПЧ 4 типов (6,11,16,18) в соскобе эпителиальных клеток урогенитального тракта методом ПЦР с детекцией в режиме «реального времени».
Количественное определение ДНК ВПЧ позволяет врачу-клиницисту подобрать оптимальную схему лечения для каждого пациента и, при необходимости контролировать эффективность терапии.
Необходимым условием получения достоверного результата исследования является соблюдение техники взятия соскоба эпителиальных клеток. В состав тестов по диагностике и мониторингу ВПЧ введен специальный параметр – контроль взятия материала (КВМ). КВМ представляет собой тест по определению количества геномной ДНК человека в биоматериале, источником которой являются эпителиальные клетки, попадающие в пробу при правильной технике взятия биоматериала.
Аналитические показатели: определяемый фрагмент – уникальная последовательность ДНК ВПЧ 6, 11, 16,18 типов. Специфичность определения – 100 %. Чувствительность определения – 100 копий ДНК ВПЧ в образце.
Литература
- Профилактика рака шейки матки: Руководство для врачей. – М.: МЕДпресс-информ, 2008.
- Полонская Н.Ю., Юрасова И.В., Сокольская Т.Ю. Преимущества и эффективность стандвртизации цитологических исследований в гинекологии // Клиническая лабораторная диагностика. – 2004. №11 с.47-50.
- Bekkers R., Meijer C., et al. Effects of HPV detection in population-based screening programmers for cervical cancer: a Dutch moment // Gynecol. Oncol. 2006; Mar: 100(3):451-4.
- Khan M., et al. The elevated 10-year risk of cervical precancer and cancer in women with human papillomavirus (HPV) type 16 or 18 and the possible utility of type specific HPV testing in clinical practice // J. nat. cancer inst. 2005; 97:1072-9.
- Snijders J., Meijer C. The value of viral load in HPV detection in screening // HPV today 2006; 8:8-9.
Накануне и в день обследования пациентке не рекомендуется выполнять спринцевание влагалища, исключить половые контакты, проведение интравагинального УЗИ, кольпоскопии. Рекомендуется брать материал не ранее, чем через 14 дней после применения антибактериальных препаратов и местных антисептиков, и не ранее, чем через 1 месяц после применения антибиотиков перорально. Не рекомендуется взятие биоматериала на фоне проведения антибактериальной терапии или применения пробиотиков и эубиотиков. Если для исследования используется соскоб из уретры, сбор материала рекомендуется проводить до или не ранее 2 – 3 часов после мочеиспускания.
При обследовании мужчин рекомендуется за 1–2 суток до взятия мазка (соскоба) исключить половые контакты. В день и накануне взятия биоматериала нельзя использовать антисептики. Перед взятием материала необходимо воздержаться от мочеиспускания в течение 1,5-2 часов до процедуры.
- Наличие папилломатозных разрастаний и изменений на слизистых оболочках половых органов.
- Контроль проводимой терапии;
- Скрининг специальных групп женщин.
Стартовый возраст для начала скрининга:
- с 21 года или в течение 3 лет после начала половой жизни;
- с 18 лет при высокой степени сексуальной активности;
- с 30 лет для новых программ (основанных на выявлении ДНК ВПЧ) или с 25 лет для существующих программ (классическое цитологическое исследование).
Специальные группы, которым показан скрининг:
- женщины, имеющие в анамнезе рак шейки матки;
- женщины в возрасте 25-65 лет, которым никогда не проводилось цитологическое исследование или проводилось более 3 лет назад;
- женщины с кровотечением в репродуктивном периоде, кровотечениями после наступления менопаузы, посткоитальными кровотечениями.
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Форма представления результатов:
Количественный результат по каждому выявляемому показателю.
Единицы измерения:
Логарифм копий ДНК ВПЧ на 105 эпителиальных клеток (Lg копий ДНК /105 эп. клеток).
Интерпретация положительного результата:
- В анализируемом образце биологического материала обнаружена ДНК, специфичная для вируса папилломы человека исследуемых типов в выявленной концентрации.
Интерпретация результата «не обнаружено»:
- В анализируемом образце биологического материала не найдено фрагментов ДНК, специфичных для вируса папилломы человека исследованных типов.
- Концентрация ДНК возбудителей в образце ниже границы чувствительности теста.
Контроль взятия материала:
Тест КВМ выполняется до проведения тестов по выявлению ДНК ВПЧ. В случае, если в пробе значение КВМ неудовлетворительное, т.е. менее 4 lg (10000) копий ДНК человека в пробе, исследование ДНК ВПЧ не проводится и рекомендуется повторное взятие биологического материала.
Источник