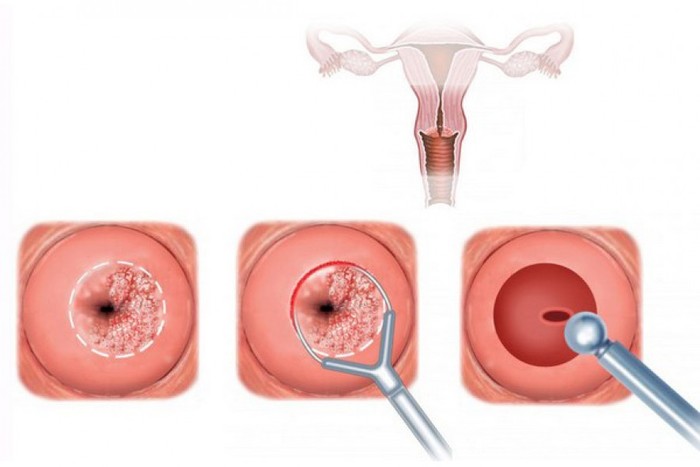
Вируса папилломы человека это
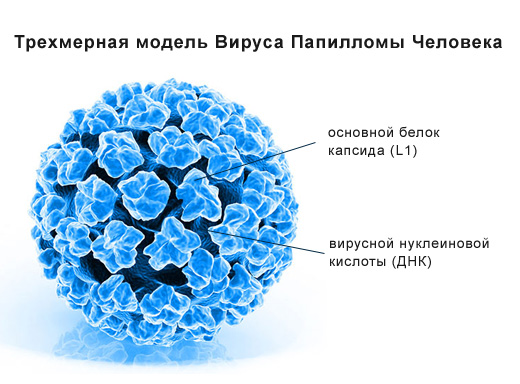
Bирус папилломы человека (ВПЧ) – чрезвычайно распространенная в мире инфекция, передаваемая половым путем.
Особенность этой инфекции заключается в том, что она может в течение многих лет никак себя не проявлять, но в итоге привести к развитию доброкачественных (папилломы) или злокачественных (рак шейки матки) заболеваний половых органов.
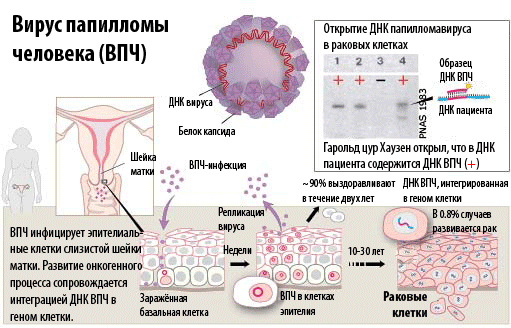
Типы вируса папилломы человека
Известно более 100 типов ВПЧ. Типы — это своеобразные «подвиды» вируса, отличающиеся между собой. Типы обозначаются номерами, которые присваивались им по мере открытия.
Группу высокого онкогенного риска составляют 14 типов: 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, 68 (эти типы имеют отношение к развитию рака шейки матки).
Кроме того, известны типы низкого онкогенного риска (главным образом, 6 и 11). Они приводят к образованию аногенитальных бородавок (остроконечных кондилом, папиллом). Папилломы располагаются на слизистой вульвы, влагалища, в перианальной области, на коже половых органов. Они практически никогда не становятся злокачественными, однако приводят к существенным косметическим дефектам в области гениталий. Бородавки на других частях тела (руки, ноги, лицо) также могут быть вызваны этими типами вируса, а могут иметь и иное происхождение. В последующих статьях будем отдельно обсуждать типы ВПЧ «высокого риска» и «низкого риска».
Заражение вирусом папилломы человека
Передается вирус, главным образом, при половых контактах. Рано или поздно заражаются ВПЧ почти все женщины: до 90% сексуально активных женщин столкнется с этой инфекцией в течение жизни.
Но есть и хорошие новости: большинство инфицированных (около 90%) избавятся от ВПЧ без каких-либо медицинских вмешательств в течение двух лет.
Это нормальное течение инфекционного процесса, вызванного ВПЧ, в организме человека. Этого времени достаточно для того, чтобы иммунная система человека полностью избавилась от вируса. В такой ситуации ВПЧ не принесет никакого вреда организму. То есть, если был обнаружен ВПЧ какое-то время назад, а сейчас его нет, это абсолютно нормально!
Необходимо учитывать, что иммунная система работает у разных людей с «разной скоростью». В связи с этим скорость избавления от ВПЧ может быть разной у половых партнеров. Поэтому возможна ситуация, когда у одного из партнеров обнаружен ВПЧ, а у другого – нет.

Большинство людей заражаются ВПЧ вскоре после начала половой жизни, и многие из них никогда не узнают о том, что были инфицированы ВПЧ. Стойкого иммунитета после заражения не формируется, поэтому возможно повторное заражение как тем же вирусом, с которым уже была встреча, так и другими типами вируса.
ВПЧ «высокого риска» опасен тем, что он может приводить к развитию рака шейки матки и некоторых других видов рака. Других проблем ВПЧ «высокого риска» не вызывает.
ВПЧ не приводит к развитию воспаления на слизистой влагалища/шейки матки, нарушениям менструального цикла или бесплодию.
ВПЧ никак не влияет на способность к зачатию и вынашиванию беременности.
Ребенку ВПЧ «высокого риска» не передается во время беременности и в процессе родов.
Диагностика вируса папилломы человека
Сдавать анализ на ВПЧ высокого онкогенного риска до 25 лет практически бессмысленно (кроме тех женщин, которые рано начинают половую жизнь (до 18 лет)), так как в это время очень велика вероятность обнаружить вирус, который вскоре самостоятельно уйдет из организма.
После 25 – 30 лет сдавать анализ имеет смысл:
- совместно с анализом на цитологию (PAP – тестом). Если есть и изменения в PAP — тесте, и ВПЧ «высокого риска», то такая ситуация требует особого внимания;
- длительная персистенция ВПЧ «высокого риска» в отсутствие цитологических изменений также требует внимания. В последнее время доказано, что чувствительность ВПЧ-тестирования в профилактике рака шейки матки выше, чем чувствительность цитологического исследования, в связи с чем определение только ВПЧ (без цитологического исследования) одобрено как самостоятельное исследование для профилактики рака шейки матки в США. Однако в России рекомендовано ежегодное цитологическое исследование, поэтому видится разумным сочетание этих двух исследований;
- после лечения дисплазии/предрака/рака шейки матки (отсутствие ВПЧ в анализе после лечения практически всегда свидетельствует об успешном лечении).
Для исследования необходимо получить мазок из канала шейки матки (возможно исследование и материала из влагалища, однако в рамках скрининга рекомендуется получение материала именно из шейки матки).
Анализ нужно сдавать:
- 1 раз в год (если ВПЧ «высокого риска» ранее был обнаружен, и анализ сдается совместно с цитологическим исследованием);
- 1 раз в 5 лет, если предыдущий анализ был отрицательным.
Сдавать анализ на ВПЧ низкого онкогенного риска нет необходимости практически никогда. Если папиллом нет, то этот анализ не имеет смысла в принципе (носительство вируса возможно, лечения вируса нет, поэтому что дальше делать с результатом анализа, неизвестно).
Если папилломы есть, то:
- чаще всего они вызваны именно ВПЧ;
- удалять их необходимо вне зависимости от того, обнаружим мы 6/11 типы или нет;
- если уж брать мазок, то непосредственно с самих папиллом, а не из влагалища/шейки матки.
Существуют тесты для выявления ВПЧ разных типов. Если вы периодически сдаете анализы на ВПЧ, обращайте внимание, какие конкретно типы включены в анализ. Некоторые лаборатории делают исследование только на 16 и 18 тип, другие – на все типы вместе. Также возможно сдать анализ, который позволит выявить все 14 типов вируса «высокого риска» в количественном формате. Количественные характеристики важны для прогнозирования вероятности развития предрака и рака шейки матки. Применяться эти тесты должны в контексте профилактики рака шейки матки, а не как самостоятельный тест. Анализ на ВПЧ без результатов цитологии (РАР-теста) чаще всего не позволяет сделать никаких выводов о состоянии здоровья пациентки.
Нет такого анализа, который позволит определить, «уйдет» ли вирус у конкретной пациентки или нет.

Лечение вируса папилломы человека
Не существует медикаментозного лечения ВПЧ. Существуют методы лечения состояний, вызванных ВПЧ (папилломы, дисплазия, предрак, рак шейки матки).
Это лечение должно осуществляться с применением хирургических методов (криокоагуляция, лазер, радионож).
Никакие «иммуностимуляторы» не имеют отношения к лечению ВПЧ и применяться не должны. Ни один из широко известных в России препаратов (Аллокин-Альфа, Изопринозин, Гроприносин и др.) не прошли адекватных испытаний, которые бы показали их эффективность и безопасность. Ни в одни протоколы/стандарты/рекомендации эти препараты не входят.
Наличие или отсутствие «эрозии» шейки матки не влияет на тактику лечения ВПЧ. Подробнее о тех ситуациях, когда надо лечить эрозию, можно почитать в статье «Эрозия или не эрозия?».
Если у пациентки нет жалоб, а также нет папиллом/изменений на шейке матки при кольпоскопии и по данным PAP — теста, никакие лечебные процедуры не нужны.
Необходимо только пересдавать анализ 1 раз в год и следить за состоянием шейки матки (ежегодно PAP — тест, кольпоскопия). У большинства пациенток вирус «уйдет» из организма самостоятельно. Если и не уйдет, совершенно необязательно, что он приведет к развитию рака шейки матки, но контроль необходим.
Лечение половых партнеров не требуется (за исключением тех случаев, когда у обоих партнеров есть папилломы половых органов).
Профилактика заражения вирусом папилломы человека
Разработаны вакцины, защищающие от 16 и 18 типов ВПЧ (одна из вакцин также защищает от 6 и 11 типов). Типы ВПЧ 16 и 18 «отвечают» за 70% случаев рака шейки матки, а потому защита от них так важна. Плановая вакцинация применяется в 45 странах мира.
Презерватив (не обеспечивает 100% защиты).
Единственный метод, обеспечивающий 100% защиту, — воздержание от половых контактов. Я ни в коем случае не агитирую за него, просто даю информацию к размышлению.
Источники:
- www.cdc.gov (официальный сайт Центра по Контролю и Профилактике Заболеваемости, США);
- www.who.int (официальный сайт Всемирной Организации Здравоохранения);
- AB Moscicki, M Schiffman, S Kjaer, LL Villa. Chapter 5: Updating the natural history of HPV and anogenital cancer. Vaccine 2006; 24: S42-51. (Данные о естественном течении папилломавирусной инфекции и аногенитального рака);
- FT Cutts, S Franceschi, S Goldie, X Castellsague, S de Sanjose, G Garnett, WJ Edmunds, P Claeys, KL Goldenthal, DM Harper, L Markowitz Human papillomavirus and HPV vaccines: a review (ВОЗ. Вирус папилломы человека и вакцины против ВПЧ. Обзор.);
- Шипулина О.Ю. Автореферат диссертации на соискание степени кандидата медицинских наук. Эпидемиологические особенности и меры профилактики онкогинекологической патологии папилломавирусной этиологии. 2013г.;
- Профилактика рака шейки матки. Руководство для врачей. Под ред. Акад. РАМН Г. Т. Сухих, проф. В.Н. Прилепской. Москва. «МЕДпресс-информ» 2012 г.;
- Stoler MH, Austin RM, Zhao C. Point-Counterpoint: Cervical Cancer Screening Should Be Done by Primary Human Papillomavirus Testing with Genotyping and Reflex Cytology for Women over the Age of 25 Years. J Clin Microbiol. 2015 Sep;53(9):2798-804. doi: 10.1128/JCM.01087-15. Epub 2015 May 6. (Скрининг рака шейки матки должен проводится с использованием ВПЧ-тестирования на первом этапе).
Источник
Читайте на Зожнике:
Смартфоны смогут диагностировать рак и папилломавирус
Рассеянный склероз: как возникает, как распознать, как лечить
Убийственные доводы: сколько жизней сохраняют прививки (инфографика)
Новое супероружие в борьбе с раком
Юлия Кудерова Среда, 05.07.2017
Источник
Как происходит заражение вирусом папилломы человека? Какой риск развития рака шейки матки при заражении ВПЧ? Что такое ВПЧ высокого онкогенного риска? На эти и другие вопросы отвечает кандидат медицинских наук акушер-гинеколог Хоперская Ольга Викторовна
Уважаемые девушки, женщины, отдельно написать о папилломавирусной инфекции решила потому, что практически каждая пациентка, столкнувшись с данной инфекцией и, прочитав в интернете, что вирус приводит к развитию рака шейки матки, испытывает страх. Переживания могут быть выраженными, вплоть до тяжелой депрессии.
А между тем, 80% женщин, живущих половой жизнью, рано или поздно сталкиваются с данной инфекцией, а многие – даже неоднократно. При этом большая часть даже не узнает о факте инфицирования, так как заболевание часто протекает бессимптомно, а профилактические осмотры в нашей стране посещают не более трети женщин. И что же, неужели всем инфицированным дамам грозит рак шейки матки? Нет!
Согласно данным статистики, из 1000 женщин, заразившихся ВПЧ, рак шейки матки развивается только у одной, и то, спустя 10 – 15 лет (подробнее – в статье Рак шейки матки).
Поэтому, главное, что мы должны с Вами сделать, если результат ВПЧ – тестирования оказался положительным, – успокоиться. Взять себя в руки нам необходимо потому, что негативные переживания и бессонные ночи подрывают работу нашей иммунной системы, так необходимой нам для борьбы с вирусом.
Три вопроса о ВПЧ, которые пациентки задают врачу-гинекологу наиболее часто
Откуда у меня взялась эта инфекция?
- половой путь передачи ВПЧ – является основным, осуществляется через непосредственный контакт кожи и слизистых оболочек, особенно при наличии в них дефектов (нетрадиционные половые контакты – не исключение);
- контактно-бытовой путь заражения – не имеет отношения к типам вируса, поражающим аногенитальную область, таким путем мы можем заразиться типами, вызывающими развитие бородавок на подошвах и кистях рук (1, 2, 4, 7, 10, 26, 27, 28, 29, 41, 57, 65, 63 типы);
- передача вируса от инфицированной матери плоду внутриутробно или во время родов.
Исходя из вышесказанного, думаю, понятно, что наличие ВПЧ в образце из цервикального канала является следствием:
- вашего рискованного сексуального поведения (частая смена половых партнеров без использования презервативов);
- рискованного сексуального поведения вашего полового партнера.
Установить точное время инфицирования часто сложно. Дело в том, что «скрытый» период ВПЧ – инфекции (т.е. времени, когда установить наличие вируса еще невозможно) колеблется в широких пределах: от 2 до 12 месяцев, чаще всего – 3 – 6 месяцев. Это значит, что проверяться на наличие ВПЧ спустя неделю и даже месяц после полового контакта с новым партнером бессмысленно: вы можете быть уже заражены, но лабораторная диагностика вируса покажет отрицательный результат. Описаны даже единичные случаи длительности «скрытого» периода в течение нескольких лет, но это крайняя редкость.
Можно ли полностью излечиться от ВПЧ?
Ответ положительный. И можно и нужно! Хорошая новость заключается в том, что здоровый организм самостоятельно излечивается от ВПЧ в течение двух лет.
На сегодняшний день не существует препаратов с доказанной противовирусной активностью, способных уничтожить вирус.
Назначаемые нами препараты обладают или противовирусным эффектом (замедляют размножение вирусов) или иммуностимулирующим действием (повышают активность собственной иммунной системы). Цель их назначения – помочь организму справиться с инфекцией. Ряд исследований подтверждают эффективность терапии.
Не всегда можно обойтись лишь наблюдением и лекарственными препаратами: в случае, если цитологическое заключение и кольпоскопическая картина говорят нам о HSIL (читайте в статьях Эрозия шейки матки, что делать? и Онкоцитология), показано физиохирургическое лечение.
Чем мне грозит данная инфекция?
После заражения ВПЧ возможны два варианта развития событий.
- В 90% случаев у здоровых людей инфицирование носит временный характер.
- В оставшихся 10% случаев вирус персистирует (продолжает оставаться в организме человека), встраивается в его геном, изменяет жизненный цикл клеток эпителия шейки матки, приводя к развитию дисплазии разной степени (9%) и рака шейки матки (1%).
Определить вариант по которому состоялось инфицирование возможно лишь по истечении двух лет, так как через год после инфицирования выздоравливают 70% пациентов, а через два – оставшиеся 20% счастливчиков.
В первом случае изменения в эпителии касаются лишь отдельных клеток (появляются койлоциты – клетки эпителия с измененным ядром и вакуолизацией, такие клетки хорошо видны при цитологическом исследовании и соответствуют заключению LSIL), а во втором происходят более глубокие изменения: нарушается слоистость эпителия ввиду размножения клеток эпителия с признаками атипии (HSIL).
Именно персистенция вируса опасна.
Конечно, возможно и спонтанное выздоровление и на этой стадии, но вероятность мала. Зато пропорционально увеличению тяжести дисплазии возрастает риск развития рака шейки матки. Поэтому тактика при HSIL, когда вирус уже встроен в геном измененных клеток, всегда включает удаление пораженной ткани.
Какие же факторы способствуют персистенции ВПЧ?
- раннее начало половой жизни;
- большое количество половых партнеров;
- ослабленный иммунитет;
- инфекции, передающиеся половым путем;
- наличие бактериального вагиноза, аэробного вагинита и вульвовагинального кандидоза;
- хронические воспалительные заболевания органов мочеполовой системы;
- курение;
- неоднократные аборты;
- нарушения менструального цикла;
- прием антибиотиков;
- высокая вирусная нагрузка и инфицирование несколькими типами ВПЧ.
Именно поэтому призываю Вас заботиться о себе, вести здоровый образ жизни, порядочную половую жизнь, использовать грамотную контрацепцию, посещать гинеколога и регулярно сдавать мазки.
Что представляет собой ВПЧ?
ВПЧ – объединенное название группы мелких вирусов, способных вызывать развитие опухолевых процессов. Сегодня нам известно более 200 типов вируса, около 40 из них вызывают заболевания аногенитальной области.
ВПЧ высокого онкогенного риска
В зависимости от частоты встречаемости при онкологических заболеваниях типы вируса подразделены на высокоонкогенные (наиболее часто обнаруживаемые) и типы с низкой онкогенностью. К ВПЧ высокого онкогенного риска относятся 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, 73, 82 типы вируса. Наибольшее значение в канцерогенезе (развитии рака) имеют 16 и 18 типы вируса, обнаруживаемые при раке шейки матки в 70% случаев.
ВПЧ способен вызывать не только рак шейки матки, в 88% случаев вирус является виновником онкологических заболеваний ануса, в 78% – влагалища, в 51% – полового члена, в 31% – ротоглотки и в 25% – вульвы. Основными виновниками рака вышеперечисленных областей также являются 16 и 18 типы ВПЧ.
Существует прививка от ВПЧ 16 и 18 типов, а также от 16, 18, 6 и 11 (подробнее читайте в статье Рак шейки матки).
ВПЧ низкого онкогенного риска
К ВПЧ с низкой онкогенностью (способностью вызывать рак) относятся 6,11, 40, 42, 43, 44, 54, 61, 72, 81 типы вируса. Так 6 и 11 типы, никогда не находят при обследовании онкологических больных, зато они чаще всего являются причиной возникновения остроконечных кондилом аногенитальной области – частой причиной обращения к гинекологу в связи с появлением косметического дефекта. Именно пациентки с кондиломами, в основном, и узнают о наличии у них папилломавирусной инфекции и очень боятся рака шейки матки, хотя им – то как раз и не о чем беспокоиться, хотя, конечно инфицирование 6 и 11 типами не исключает наличие сопутствующего инфицирования высокоонкогенным ВПЧ.
Аногенитальные бородавки
Являются наиболее распространенным клиническим проявлением ВПЧ-инфекции. Сами по себе, как уже было сказано, они практически всегда безопасны для здоровья, но доставляют немало беспокойств их «счастливому» обладателю за счет неэстетичного косметического эффекта. В 2014 году показатель заболеваемости в Российской Федерации составил 21,8 случаев на 100 000 населения.
В 90% случаев аногенитальные бородавки бывают вызваны 6 и 11 типами ВПЧ, но их наличие – показание к обследованию на наличие ВПЧ высокого канцерогенного типа.
Период между инфицированием вирусом и возникновением бородавок в среднем составляет 6 месяцев у женщин и 10 – 11 – у мужчин. Основной путь передачи ВПЧ 6 и 11 типов также половой, хотя возможны случаи инфицирования контактно-бытовым путем при несоблюдении правил личной гигиены. Диагностика аногенитальных бородавок не представляет особых сложностей – картина вполне показательна, а вот идентификация типа ВПЧ производится молекулярно-биологическим методом, позволяющим определить вирусную нагрузку.
Чаще всего аногенитальные бородавки представляют собой пальцеобразные небольшие безболезненные образования, расположенные на слизистой оболочке или коже наружных половых органов (остроконечные кондиломы, рисунок 1), или возвышения над поверхностью кожи в виде папул (рисунок 2), чаще небольших размеров, цвет их может не отличаться от подлежащего кожного покрова, но может быть и значительно темнее. Также возможны проявления в виде пятен, расположенных на слизистой оболочке половых органов, различного цвета – от серо-белого до красно-коричневого.
Излюбленное месторасположение – слизистая оболочка малых половых губ, вульвы, влагалища, шейки матки, выходного отверстия уретры. Возможно расположение в области больших половых губ и вблизи анального отверстия. У мужчин очаги поражения локализуются на головке полового члена, уздечке, венечной борозде, внутренней поверхности крайней плоти, в области отверстия мочеиспускательного канала, теле полового члена, коже мошонки, в аногенитальной и паховой областях.
Рисунок 1 – Остроконечные кондиломы слизистой оболочки
Рисунок 2 – Папилломы кожных покровов
Количество аногенитальных бородавок также может быть различным: при здоровой иммунной системе они единичны, не беспокоят человека ничем, кроме самого факта своего присутствия (что, кстати, может довести человека до нервного истощения), и могут самостоятельно пройти без каких-либо медицинских вмешательств в течение нескольких месяцев – двух лет (так же, как и кожные бородавки иной локализации). Но в случае иммунодефицита возможно разрастание большого количества бородавок, они могут сливаться, приобретая вид «цветной капусты» и доставлять выраженный дискомфорт: зуд, жжение, болезненность, образование трещин и даже кровоточивость слизистой или кожного покрова в месте поражения.
Гигантская кондилома Бушке-Левенштайна
Крайне редко возможно образование гигантской кондиломы Бушке — Левенштайна (рисунок 3), представляющей собой последствие сливного роста папиллом, образующих широкое основание, над которым возвышаются «капустоподобные» ворсинчатые разрастания, такая опухоль, хоть и считается доброкачественной, но все же может со временем озлокачествляться.
Рисунок 3 – Гигантская кондилома Бушке — Левенштайна
Удаление аногенитальных бородавок
Удаление бородавок проводится следующими методами:
- физическими (электрокоагуляция, лазерная деструкция, радиохирургическая деструкция, криодеструкция);
- химическими;
- цитотоксическими методами;
- хирургическим путем.
Возможно применение иммуномодуляторов местного действия, а при длительном рецидивирующем (от латинского «recidere» – «возвращаться», повторяющиеся эпизоды заболевания) течении – интерферонов системного действия, а также внутриочаговое введение препаратов α-интреферона. Гистологическое исследование всегда желательно (но не при любом методе удаления возможно) для вашего же спокойного сна.
Искренне желаю каждой девушке, женщине быть здоровой! Надеюсь, что вы читали мою статью с целью самообразования и расширения кругозора, а знание – сила!
Источник