Вирус папилломы человека высокого канцерогенного риска тип впч 31

По данным Всемирной организации здравоохранения, в настоящее время ежегодно регистрируется более полумиллиона случаев развития рака шейки матки. Около 250 тысяч женщин погибают от этой болезни из-за слишком поздней диагностики и неэффективного лечения. Вирус папилломы человека является одним из наиболее опасных онкогенных вирусов, провоцирующих развитие злокачественных опухолей.
Что это такое?
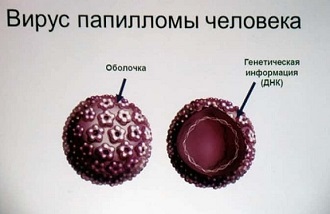 ВПЧ – название для объединенного семейства вирусов, включающего в себя более 100 различных видов. Все эти штаммы разделены по степени онкогенного риска. Около 13 штаммов приводят к возникновению различных видов рака. При излечении от вируса, человек может инфицироваться повторно.
ВПЧ – название для объединенного семейства вирусов, включающего в себя более 100 различных видов. Все эти штаммы разделены по степени онкогенного риска. Около 13 штаммов приводят к возникновению различных видов рака. При излечении от вируса, человек может инфицироваться повторно.
Виды вируса
По статистике, больше половины населения России являются носителями разных видов вируса, что показывает огромную распространенность вируса. Но это не значит, что ВПЧ для всех становится смертельным диагнозом. Многие типы папилломавируса никак не отражаются на здоровье человека, и приносят только эстетические дефекты в виде папиллом и бородавок.
Существуют такие штаммы вируса, при которых развитие рака практически невозможно, так называемый ВПЧ низкого онкогенного риска. Также широко распространены виды среднего онкогенного типа, и эти две категории включают в себя большинство разновидностей папилломавируса.
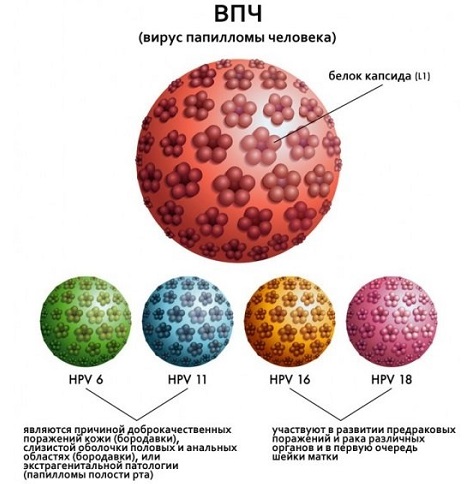
Видов вируса, провоцирующих возникновение злокачественных опухолей, значительно меньше. Сюда включаются 31, 33, 6, 11, 16 и 18 типы. Последние два представляют большую угрозу для женщин. Сегодня с помощью многочисленных исследований достоверно установлена связь между развитием рака шейки матки и инфицированием 16 и 18 типом ВПЧ. В 70% случаев именно с разрушительным воздействием инфекции связано появление злокачественных новообразований. Рак шейки матки стоит на втором месте по наиболее распространенным видам рака среди женщин.
Уже в первые два года после попадания вируса в организм у 15-30% женщин происходят изменения в области шейки матки, и возникает предраковое состояние. За это же время такие изменения возникают лишь у 2% женщин, незараженных ВПЧ.
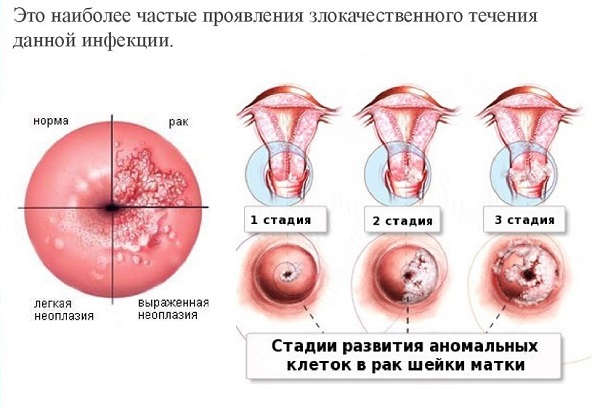
16 и 18 типы опасны полным отсутствием внешних проявлений. Только соответствующие анализы могут указать на наличие папилломовируса, в то время как сама инфекция протекает бессимптомно. Даже при обычном осмотре у гинеколога выявить заражением этими типами вируса невозможно. Такое проявление вируса называется латентной формой и без лечения может привести к развитию онкологии.
Способы передачи

Наиболее распространенным путем передачи являются незащищенные половые контакты с носителями ВПЧ. Риск заразиться вирусом в первые три года после первого полового контакта составляет 46%. Именно поэтому к группам, традиционно находящимся в зоне риска, например, проституткам, добавляются те женщины и девушки, у которых может быть только один половой партнер. В частности, высокий процент инфицированных встречается среди подростков. Заражение может произойти при любом виде полового контакта, в том числе анального и орального.
Другой способ заражения – инфицирование новорожденных, проходящих через родовые пути. Если будущая мама является носителем ВПЧ, ребенок имеет высокий шанс подхватить вирус при естественных родах. Впоследствии у таких детей может развиваться папилломатоз гортани – вирусное заболевание, характеризующееся возникновением папиллом в гортани. Поэтому перед планированием беременности женщине необходимо вылечить инфекцию, если она присутствует.
Известен и контактно-бытовой путь заражения. Это может произойти через маленькие кожные раны при тесном контакте. Например, при использовании общих предметов гигиены, посещении спортзала или бассейна. При этом такой путь передачи не может привести к инфицированию высокоонкогенным типом ВПЧ. Зато этим способом вполне можно заразиться кожными бородавками.
Как происходит заражение
 ВПЧ инфицирует многослойный эпителий, что и определяет область поражения – кожа и слизистые оболочки. ДНК вируса стремится проникнуть в ядро клетки человека. Её целью является воспроизводство там онкогенных белков. После того, как это происходит, они начинают стремительно реплицироваться. Если это доброкачественный рост, то клетки не выходят за пределы эпителия. Если злокачественный, распространение патологического процесса запускает возникновение метастаз. При этом инкубационный период длится около трех месяцев.
ВПЧ инфицирует многослойный эпителий, что и определяет область поражения – кожа и слизистые оболочки. ДНК вируса стремится проникнуть в ядро клетки человека. Её целью является воспроизводство там онкогенных белков. После того, как это происходит, они начинают стремительно реплицироваться. Если это доброкачественный рост, то клетки не выходят за пределы эпителия. Если злокачественный, распространение патологического процесса запускает возникновение метастаз. При этом инкубационный период длится около трех месяцев.
Проявления ВПЧ
- Бородавки. Плотные наросты, имеющие неровные поверхность и цвет от серого до черного. Появляются после заражения низкоонкогенными типами вируса. Не угрожают жизни и здоровью человека, но вызывают косметические проблемы. Чаще всего локализуются в районе рук и стоп, но также могут появляться на поверхности всей кожи. Существуют также подошвенные бородавки, которые уплотняются и грубеют при ходьбе. Их характерное отличие – появление крови при срезании верхушки.
- Остроконечные кондиломы. Являются доброкачественными новообразованиями, располагающимися на коже и половых органах. Встречаются наросты телесного, розового или коричневого цвета. Их характерной особенностью является быстрое распространение. Могут возникать в области шейки матки, но не исключено и поражение мочеиспускательного канала, а также прямой кишки и ануса. Кондиломы доставляют дискомфорт в виде зуда и жжения. На ранней стадии чаще всего появляются одиночные наросты. На более поздних стадиях кондиломы показывают способность к слиянию. Не представляют опасности перерождения в злокачественные новообразования.
- Плоские кондиломы. Более опасны в плане развития онкологии. Вероятность рака увеличивается с возникновением новых наростов. Этот вид кондилом обычно располагается на слизистой оболочке влагалища.
- Бовеноидный папулез. Вирусное заболевание, считающееся предраковым. Характерная особенность – сыпь в области половых органов. Также возникают пигментные папулы – гладкие образования коричневого цвета. Папулы часто появляются вместе с кондиломами и бородавками. Компоненты сыпи могут привести к разным видам рака, опасным женщин.
- Рак шейки матки. Для каждой женщины существует риск того, перерождения вируса в хроническую форму, а предраковое состояние в итоге может перерасти в рак. Если не заниматься лечением вируса, то это станет просто вопросом времени. У женщин с хорошим иммунитетом такие процессы происходят за 15 лет. У тех, чей организм страдает от ослабления иммунитета, например, у ВИЧ положительных женщин, на это потребуется всего 5 лет.
Диагностика заболевания
Нередко случается так, что женщина может обнаружить проблемы в организме после обычного визита к гинекологу, где у нее возьмут мазок. Чтобы выявить причины возможных заболеваний, врачу приходится проводить ряд дополнительных исследований и тестов.
Итак, порядок диагностики заболевания должен быть следующий:
- Первичный внешний осмотр врача, на котором берется мазок для определения состояния микрофлоры влагалища, уровня лейкоцитов и выявления заболеваний.
- Если результаты анализа пришли неудовлетворительные, о чем будет говорить повышенный уровень лейкоцитов, гинеколог назначает дополнительные анализы на ЗППП, в число которых обязательно входит несколько штаммов ВПЧ. В частности, используется ПЦР анализ, помогающий установить не только наличие вируса в организме, но и его типы. Совместно с ПРЦ делается количественный тест, диагностирующий уровень концентрации вируса. Этот показатель, а также количество новообразований влияют на возможность появления онкологии.
- Когда результат показывает один или несколько типов ВПЧ, женщине назначается кольпоскопия. Это процедура осмотра шейки матки с помощью кольпоскопа – аппарата, предназначенного для многократного увеличения. Таким образом проводится детальное исследование шейки матки, влагалища и вульвы. С помощью кольпоскопии можно оценить, насколько вирус успел повлиять на состояние шейки матки, выявить очаги поражения, просмотреть наличие предраковых изменений и генитальных бородавок. Обычно гинеколог проводит расширенную кольпоскопию с использованием химических веществ для выявления атипичных очагов.
- При диагностике ВПЧ назначается лечение, соответствующее типу вируса и его проявлениям.
Лечение папилломовируса
 Вирус папилломы человека может длительное время скрыто присутствовать в организме носителя и при этом никак не проявлять себя. Его развитие останавливает иммунная система, которая должна тормозить распространение чужеродной ДНК. Именно на поддержание и активизацию иммунитета направлено одно из направлений лечения. Такой метод называется консервативным и включает в себя назначение иммуномодулирующих и противовирусных препаратов (Изопринозин, Аллокин-альфа и другие).
Вирус папилломы человека может длительное время скрыто присутствовать в организме носителя и при этом никак не проявлять себя. Его развитие останавливает иммунная система, которая должна тормозить распространение чужеродной ДНК. Именно на поддержание и активизацию иммунитета направлено одно из направлений лечения. Такой метод называется консервативным и включает в себя назначение иммуномодулирующих и противовирусных препаратов (Изопринозин, Аллокин-альфа и другие).
Другое направление направлено на устранение последствий инфекции: удаление возникших папиллом и кондилом. Для этого существует несколько способов:
- Хирургическое вмешательство. Представляет собой операцию по срезанию новообразований. Процедура проводится под местным наркозом. Недостатками этого метода является не только возможные последствия в виде шрамов, но и риск кровопотери. Кроме того, такой способ не дает гарантии удаления всех клеток папилломовируса.
- Электрокоагуляция. Наиболее распространенный метод удаления папиллом и бородавок за счет дешевизны и доступности. Проводится с помощью высокочастотного тока, точечно воздействующего на наросты. Как и предыдущий способ, оставляет на теле следы от удаленных папиллом. Также не гарантирует отсутствие рецидивов.

- Лазерная деструкция. Один из наиболее современных способ удаления папиллом. Для этого используется лазерный луч, который полностью убирает клетки папилломы, воздействуя на атипичные ткани. Такой метод считается наиболее надежным и безопасным. Не оставляет нежелательных последствий в виде рубцов и шрамов, сразу запаивает сосуды, чтобы предотвратить кровотечение.

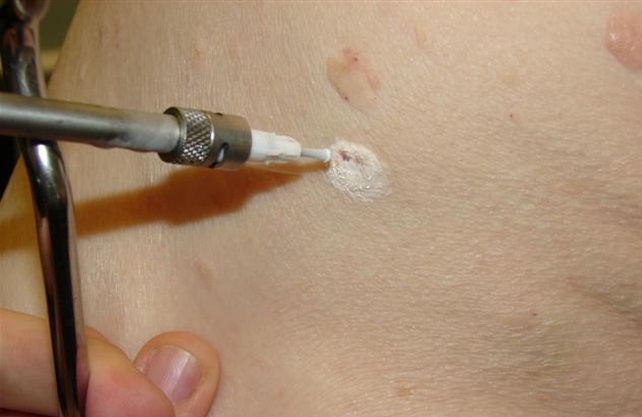
- Криодеструкция. Процедура проводится с помощью жидкого азота, который наносится на специальный аппликатор. Под воздействием жидкого азота нарост постепенно отпадает. Однако при таком методе возможно получение ожогов, что в конечном итоге даст нежелательный рубец. Это происходит из-за глубоко воздействия вещества на кожу.
Профилактика ВПЧ
Профилактика этого заболевания сводится к нескольким простым правилам:
- Использование презервативов в качестве средства контрацепции при половом акте. Этот пункт особенно важен, так как половой путь передачи инфекции наиболее распространенный.
- Осмотр у гинеколога. Женщинам раз в полгода нужно проходить осмотр у врача и сдавать мазок, чтобы знать о состоянии своего организма.
- Поддержание иммунитета. Именно иммунная система дает основной отпор папилломовирусу, и хороший иммунитет может подавить его проявления еще до того, как инфекция разовьется.
 К неспецифическим методам профилактики относится прививки против ВПЧ высокоонкогенных типов. Эти вакцины защищают от 16 и 18 типа и могут обеспечить некоторую защиту от других типов вируса. Успешно прошедшие клинические испытания, вакцины считаются безопасными и эффективными. Однако вакцинация должна производиться до первого полового контакта, потому что она только препятствует проникновению вируса в организм, но никак не сможет вылечить уже имеющуюся инфекцию. Ими рекомендуется вакцинировать девочек в возрасте с 10 до 13 лет.
К неспецифическим методам профилактики относится прививки против ВПЧ высокоонкогенных типов. Эти вакцины защищают от 16 и 18 типа и могут обеспечить некоторую защиту от других типов вируса. Успешно прошедшие клинические испытания, вакцины считаются безопасными и эффективными. Однако вакцинация должна производиться до первого полового контакта, потому что она только препятствует проникновению вируса в организм, но никак не сможет вылечить уже имеющуюся инфекцию. Ими рекомендуется вакцинировать девочек в возрасте с 10 до 13 лет.
О том что такое онкогенный ВПЧ у женщин и к чему он может привести смотрите в нашем видео:
Источник
Папилломавирус человека (ВПЧ), Human papillomavirus (HPV) принадлежит к семейству паповавирусов (Papovaviridae), роду папилломавирусов. Это ДНК-содержащий мелкий вирус, термостабильный. Является самой распространенной инфекцией, передающейся половым путем: по некоторым данным, в молодом возрасте отмечается инфицирование до 80% населения. Вирус проявляет тропность к эпителию кожи, слизистых оболочек гениталий и других органов (гортань, ротовая полость, слизистая конъюнктивы).
Основной путь передачи — половые контакты, включая анальный, оральный секс, к сожалению, использование презервативов не защищает от инфицирования данным вирусом. Возможна передача при тесном контакте кожи, слизистых оболочек с инфицированными областями. Важным фактором инфицирования новорожденного с последующим развитием респираторного папилломатоза гортани является инфицирование при прохождении по половым путям во время родоразрешения. На сегодняшний день известно более 100 видов вируса папилломы человека (ВПЧ) и из них более 40 могут вызвать поражение аногенитального тракта (половые органы и задний проход) мужчин и женщин и появление остроконечных кондилом. Папилломавирусы можно разделить на 3 основные группы:
неонкогенные ВПЧ (1, 2, 3, 5 генотипы);
низкого канцерогенного риска (НКР) ВПЧ (6, 11, 42, 43, 44 генотипы);
высокого канцерогенного риска (ВКР) ВПЧ (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 и 68 генотипы).
ВПЧ низкого канцерогенного риска (ВПЧ НКР): группа вирусов, которая приводит к доброкачественным поражениям, представлена 5 генотипами, но основными являются 6 и 11, которые составляют до 90% всех случаев инфицирования данными вирусами. Наиболее частые клинические проявление ВПЧ НКР- это остроконечные кондиломы (Condylomata acuminata). Также выделяют еще разновидности остроконечных кондилом: кератотические бородавки с локализацией на сухой коже, папулезные бородавки с локализацией на полностью ороговевшем эпителии, гигантская кондилома Бушке-Левенштейна (встречающаяся у больных сниженным клеточным иммунитетом или при беременности). Эндоуретральные кондиломы локализуются в уретре, часто сочетаются с обычными кондиломами и встречаются преимущественно у мужчин. Кондиломы шейки матки часто сочетаются с генитальными кондиломами: экзофитные кондиломы, эндофитные (плоские).
ВПЧ высокого канцерогенного риска (ВПЧ ВКР): группа типов высокого канцерогенного риска представлена 15 генотипами, наиболее распространенными из которых являются десять: 16, 18, 31, 33, 35, 39, 45, 52, 58, 59. При этом на долю 16 и 18 типов приходится 70% всех случаев инфицирования, и именно данные типы характеризуются высоким канцерогенным потенциалом, в отношении 18 генотипа наблюдается высокая частота выявления при аденокарциномах. На сегодняшний день доказана роль ВПЧ в развитии рака шейки матки, большей доли рака заднего прохода (около 90% случаев), около 40% всех случаев рака влагалища, вульвы, полового члена, 10–15% случаев рака ротовой полости и гортани.
Вирусная ДНК способна персистировать в клетке в двух формах: эписомальной (продуктивная стадия) и интегрированной (интегрированная стадия). На эписомальной стадии происходит усиленная продукция новых вирусов, что способствует вовлечению в патологический процесс новых клеток, однако клетки не теряют контроль над процессами апоптоза и эта стадия характеризуется доброкачественными изменениями со стороны эпителия. Интегрированная стадия — это стадия, когда вирус встраивается в геном клетки и приводит к суперэкспрессии онкобелков Е6, Е7, ассоциируется с предраковыми изменениями и требует соответствующей тактики лечения пациента.
Инфекция, вызываемая вирусом папилломы человека, имеет ряд важных особенностей, без учета которых использование ВПЧ-тестирования сопряжено с рядом трудностей в трактовке результатов.
С одной стороны:
ВПЧ является самой распространенной ИППП (до 80% лиц молодого возраста инфицированы данным вирусом);
при инфицировании большинство женщин (около 80%) излечиваются от ВПЧ в течение 9–15 месяцев от момента заражения без проведения лечебных процедур (т. е., при повторении теста на генотипирование через год возможно исчезновение выявленного ранее генотипа ВПЧ или изменение спектра генотипов). С возрастом способность к самоэлиминации значительно снижается;
инфицирование ВПЧ и заболевание — НЕ СИНОНИМЫ! Инфекция приводит к развитию предрака у малой части инфицированных женщин (около 0,5%);
от заражения до развития предрака и РШМ, в среднем, проходит 10–20 лет. С возрастом способность к элиминации вируса снижается, соответственно, повышается риск развития предрака и рака;
отсутствуют эффективные методы лечения на стадии латентной инфекции (нет изменений в цитологической и/или кольпоскопической картине, но выявляется вирус).
С другой стороны:
ВПЧ является основной причиной рака шейки матки. Инфицированные женщины имеют в 300 раз более высокий риск развития рака. Разработаны не только методы вторичной профилактики (цервикальный скрининг для выявления предраковых стадий), но и первичной — вакцинация девочек и мальчиков в возрасте 9–12 лет;
инфекция коварна и довольно часто не вызывает никаких жалоб у пациента и не выявляется при осмотре до перехода в стадию инвазивного рака;
клинические проявления папилломавирусной инфекции высокого риска могут маскироваться другими заболеваниями урогенитального тракта, что не позволяет вовремя выявить их с использованием традиционных методов.
Из перечисленных особенностей папилломавирусной инфекции следует, что:
1. Положительный результат тестирования на наличие вируса должен трактоваться как:
принадлежность пациента к группе высокого риска по развитию рака шейки матки;
потребность в дополнительных тщательных диагностических процедурах для выяснения текущей стадии инфекции, исключения тяжелой дисплазии и рака шейки матки;
необходимость в наблюдении за инфекцией (персистенцией) при отсутствии клинических или субклинических проявлений.
2. Отрицательный результат тестирования трактуется как отсутствие риска развития тяжелой дисплазии и рака.
Лабораторная диагностика. Диагностика ВПЧ инфицирования определяется клиническими проявлениями и клиническими задачами прогноза риска развития ВПЧ-ассоциированных злокачественных новообразований.
Лабораторные методы диагностики ВПЧ инфекции:
прямые методы: оценка наличия койлоцитов в цитологических мазках (низкая диагностическая чувствительность); выявление наличия маркеров пролиферации р16/ki 67; молекулярные методы (ПЦР анализ), которые проводятся в формате качественного и количественного тестирования с возможностью генотипирования, определение генотипов НКР и ВКР ВПЧ;
серологические методы не используются для диагностики ВПЧ инфекции.
Стратегии использования ВПЧ-тестов в диагностике предрака и рака шейки матки:
входит в комплекс цервикального скрининга: в качестве теста сортировки патологических ПАП тестов у женщин до 30 лет; тест совместно с цитологическим исследованием для всех женщин старше 30 лет. В данном случае наличие инфицирования ВПЧ (особенно, 16 и 18 генотипом, с высокой вирусной нагрузкой) позволяет прогнозировать высокий риск наличия или развития РШМ, что определяет необходимость дополнительных обследований. В случае отрицательных результатов ВПЧ тестирования, периодичность скрининга может быть увеличена до 3–5 лет (в разных странах действуют различные рекомендации) при условии отсутствия изменений в цитологическом исследовании;
рекомендован в некоторых странах как тест первичного скрининга на РШМ у женщин старше 30 лет;
контроль эффективности лечения дисплазий (первое исследование проводится через 6 месяцев после лечения совместно с ПАП тестом). При этом в случае получения положительных результатов ВПЧ теста и нормальной цитологии, необходимо дополнительное обследование, т. к. риск наличия или развития патологии высокий.
Различные методы молекулярной диагностики (ПЦР анализа) позволяют решить различные диагностические задачи:
качественный формат позволяет выявить наличие инфицирования, однако не позволяет оценить клинически значимые количества вируса, которые ассоциируются с высоким риском наличия предраковых поражений;
количественный формат позволяет выявить вирус, определить вирусную нагрузку. Это позволяет оценить не только степень риска, но и возможное уже наличие предраковых изменений, т. к. высокая вирусная нагрузка ассоциируется с реализацией онкогенного потенциала вируса. При правильном и стандартизированном заборе клинического материала вирусная нагрузка менее 105 геномных эквивалентов (ГЭ) ВПЧ ВКР в соскобе (Josefsson et al, 2000; van Duin et al, 2002; Dalstein et al, 2003; Snijders et al, 2003; Moberg et al, 2004, 2005) или 103 ГЭ приходящихся на 100 тыс. клеток человека считается клинически малозначимой, так как практически не встречается при тяжелой дисплазии и РШМ, а также ассоциирована с минимальным риском их развития. Напротив, количество вируса более 105 ГЭ, приходящихся на 100 тыс. клеток при установленном факте персистентного течения инфекции (ВПЧ выявляется более 1 года), обозначается как повышенная нагрузка ВПЧ и ассоциировано с повышенным риском развития тяжелой дисплазии и чаще встречается при РШМ. Наконец, определенной информацией обладает мониторинг вирусной нагрузки. Так, считается, что снижение количества ДНК ВПЧ более чем на 1 lg может являться маркером транзиторной инфекции. Рост вирусной нагрузки через 3, 6 и 9 мес. после проведенного лечения свидетельствует о возможности рецидива.
Генотипирование ВПЧ дает дополнительные возможности определения прогноза течения заболевания. Необходимость генотипирования может быть оправдана, т. к.:
выявление нескольких генотипов вируса ассоциировано с менее благоприятным прогнозом течения заболевания и более высоким риском персистенции;
степень онкогенности различных генотипов высокого риска не одинакова. Наибольшей онкогенностью обладают 16 и 18 типы ВПЧ, существуют рекомендации по проведению определения этих двух генотипов вируса после теста на широкий спектр типов с целью более агрессивной тактики ведения пациентов: при выявлении 16 и 18 генотипов рекомендуется сразу проводить кольпоскопическое обследование, при выявлении других типов высокого риска — сначала проводить цитологию, и только при положительном результате цитологии проводить кольпоскопию;
проведение генотипирования позволяет отличить реинфицирование от персистирования инфекции при повторном визите пациента. Получать подобную информацию тем более важно, так как опасность представляет именно хроническая персистентная форма инфекции, недавнее же инфицирование, наиболее вероятно, спонтанно излечивается. О реинфицировании говорит изменение спектра генотипов, о персистирующей инфекции — сохранение генотипа вируса через год после первого тестирования; повторное инфицирование тем же генотипом вируса после самостоятельного излечения практически невозможно.
Источник

