Пцр впч в реальном времени
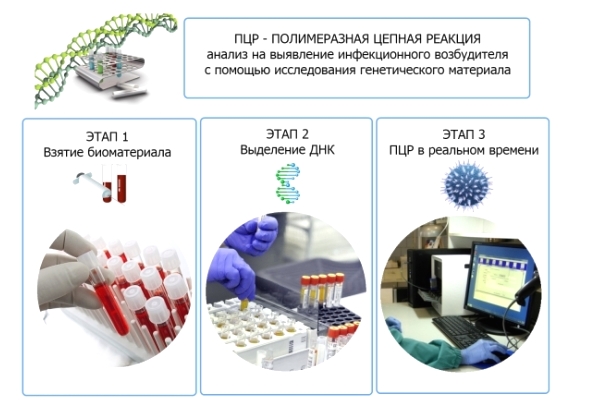
Вирус папилломы человека (ВПЧ) – распространенное заболевание, протекание которого носит хронический характер и чревато рецидивами. Полимеразная цепная реакция (ПЦР) – один из самых современных способов диагностики папилломавируса. Этот способ считается надежным и позволяет выявить не только наличие вируса в организме, но также его тип и количество. ПЦР чувствителен даже к неактивной форме вируса, при которой отсутствуют внешние проявления в виде папиллом и кондилом.
Общие сведения
 Анализ строится на исследовании ДНК пациента с целью обнаружения в ней присутствия чужеродных элементов. Любая ДНК строится на основе четырех нуклеотидов, располагающихся в определенной последовательности. Когда в организм попадает вирус, происходит изменение порядка в этой цепи, что позволяет оперативно отследить деятельность даже незначительных инородных частиц. Метод ПЦР диагностики проводится с использованием вирусных частиц, что обусловливает быстрое деление клеток.
Анализ строится на исследовании ДНК пациента с целью обнаружения в ней присутствия чужеродных элементов. Любая ДНК строится на основе четырех нуклеотидов, располагающихся в определенной последовательности. Когда в организм попадает вирус, происходит изменение порядка в этой цепи, что позволяет оперативно отследить деятельность даже незначительных инородных частиц. Метод ПЦР диагностики проводится с использованием вирусных частиц, что обусловливает быстрое деление клеток.
Такая диагностика способна отследить активность ВПЧ не только в момент его протекания в скрытой фазе, но и в инкубационный период, когда папилломавирус еще не успел заявить о себе. ПЦР позволяет выявить:
- наличие ВПЧ;
- штаммы, которыми инфицирован больной;
- количественное содержание вируса в организме.
Большинство людей инфицированы папилломавирусом, однако сильный иммунитет подавляет его проявления и не дает размножаться. Поэтому обнаружение ВПЧ качественным методом может быть не всегда оправдано. Это не рационально в случае, если вирус присутствует в организме, но его воздействие минимально и никак не вредит человеку. Тем не менее качественный анализ покажет положительный результат, чем может вести пациента в замешательство.
Поэтому для диагностики чаще всего применяют количественный метод, позволяющий отследить количество вируса в организме и определить, насколько опасна его деятельность. Кроме того, важно установить штамм ВПЧ. Они делятся по степени онкогенности: одни совершенно безопасны и способны вызывать только косметические проблемы, другие могут стать причиной возникновения рака.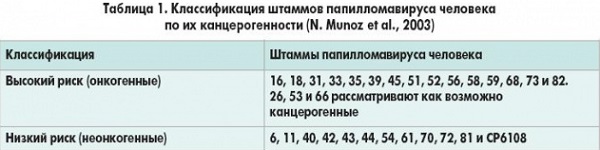
Каждая ситуация требует индивидуального подхода, поэтому прежде чем сдавать анализ, желательно проконсультироваться с врачом. Он подскажет, каким методом и на какие штаммы лучше всего проверяться, исходя из состояния пациента.
Показания для анализа
Инфицирование ВПЧ возможно только при непосредственном контакте с зараженным человеком. Вирус попадает в кровь и начинает размножение в области верхних слоев кожи, что обусловливает появление его характерных признаков – возникновение папиллом и кондилом. 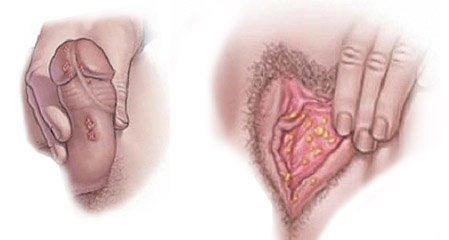 ВПЧ распространяется следующими путями:
ВПЧ распространяется следующими путями:
- при незащищенных половых контактах;
- при естественных родах от инфицированной матери к ребенку;
- контактно-бытовым путем через предметы общего пользования, личные вещи, одежду и т.д.;
- во время тесного контакта с кожей больного.
Чаще всего диагностировать ВПЧ приходят люди, у которых видны внешние признаки болезни. Однако если они никак не проявляются, это не является гарантией отсутствия вируса. Он также может присутствовать в крови и развиваться бессимптомно. Это особенно характерно для высокоонкогенных типов вируса: 16 и 18 штамма, которые провоцируют возникновение рака. Направление на диагностику этих типов обычно происходит при обращении к профильным специалистам: гинекологу и урологу. 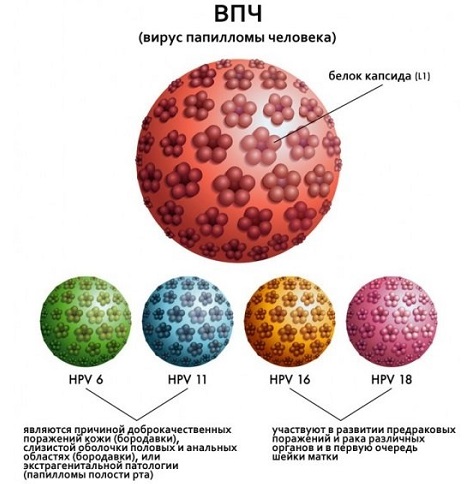
Преимущества метода
ПЦР считается одним из главных методов диагностики и остается самым востребованным среди врачей. Он используется не только для выявления ВПЧ, но также помогает обнаруживать другие заболевания, передающиеся половым путем, гепатиты, скрытые инфекции и т.д. ПЦР диагностика обладает рядом преимуществ по сравнению с другими методами выявления заболеваний. Среди них:
- Высокая специфичность. Тест помогает с большой вероятностью отделить следы чужеродной ДНК от ДНК человека в рамках собранного материала.
- Высокая производительность. ПЦР представляет собой автоматизированный процесс, помогающий провести диагностику непосредственно в день сдачи анализа. Такая скорость исследования позволяет пациенту не волноваться о результате на протяжении долгого времени и получить результат уже через несколько дней.
- Возможность сделать сразу несколько анализов. На основании одного собранного образца можно провести диагностику для выявления нескольких заболеваний. Например, одновременно можно выявить возбудителя хламидиоза и гонореи. При этом такая процедура не сможет отрицательно повлиять на достоверность результата.
- Высокая чувствительность. Тест позволяет обнаружить деятельность вируса даже в инкубационный период, когда его концентрация очень мало. Это поможет предупредить развитие патологического процесса и начать своевременное лечение.
Недостатки метода
Существуют, однако, и некоторые отрицательные моменты в проведении ПЦР диагностики. Главный из них – возможность получения ложноположительного результата. Это происходит в случае, если лечение уже проведено, инфекция побеждена, но мертвые клетки еще остаются внутри тканей. Для обновления клеток необходимо время.
Если провести анализ раньше 2-3 месяцев, ПЦР может показать положительный результат, в действительности принимая уже мертвые клетки за живые. Метод не делает различий между ними, он нацелен на поиск ДНК вируса, которую может найти даже в уже отмерших клетках. Все это приводит к получению ложноположительного результата. Избежать такой ситуации можно, если сдавать анализ в установленный лечащим врачом срок.
Также существует риск ложноотрицательного результата. В этом случае пациент никак не может повлиять на качество диагностики, так как ложноотрицательный анализ – просчет лаборатории. Он может возникнуть если:
- собранный материал неправильно транспортировался и хранился;
- нарушается стерильность, и в полученные пробы попадают другие микроорганизмы;
- реагенты были непригодными.
Для того чтобы исключить возможность получения ложноотрицательного результата, необходимо выбирать проверенную лабораторию с квалифицированным персоналом.
Виды методик
В рамках проведения ПЦР диагностики разработаны четыре метода тестирования. Каждый из них имеет свои особенности проведения и назначается, исходя из состояния пациента. Для выбора наилучшего способа необходимо проконсультироваться с врачом.
Качественный способ
Этот метод применяется для того, чтобы подтвердить или опровергнуть факт присутствия вируса в организме. Его основной недостаток – невозможность установить штамм ВПЧ (только 14-21 виды). Чаще всего качественный способ используется вместе с другими методами выявления папилломавируса. Результат при этом передается с помощью 2 оценок: «обнаружено» или «не обнаружено». То есть метод либо констатирует факт наличия чужой ДНК, либо показывает ее отсутствие.
Генотипирование
Методика способна определить как просто наличие вируса в организме, так и установить его вид. Этот способ применяют, когда необходимо установить, осталась ли вирусная ДНК после лечения или случился рецидив вследствие нового заражения. Генотипирование позволяет оценить эффективность проведенного лечения посредством определения вида вируса. Если этот тот же штамм, от которого лечился больной, значит, терапия прошла безуспешно. Если же исследование показывает другой вид ВПЧ, можно говорить о повторном заражении. Результат также представлен формулировками «обнаружено» или «не обнаружено».
Комбинированный метод
Узкоспециализированный способ диагностики, основанный на соединении качественного метода и определения 16 штамма посредством генотипирования. Результат представлен 3 ответами: «не обнаружено», «обнаружен 16 штамм», «обнаружен ВПЧ с 16 типом включительно». Этот метод применяется при подозрении на наличие высокоонкогенного типа папилломавируса, способного вызывать у женщин рак шейки матки.
Количественный метод
Такой способ позволяет установить концентрацию вируса в организме и отследить развитие ВПЧ. Считается наиболее информативным, так как позволяет определить тяжесть протекающего процесса, исходя из которой, подбирается лечение. Основан на определении количества вирусных клеток в рамках исследуемых 100 тысяч. Когда их совокупность превышает 5, это свидетельствует о высокой концентрации папилломавируса, что повышает возможность появления раковых клеток. Если количество клеток меньше 3, концентрация указывается как незначительная.
Как сдавать анализ
Специальной подготовки для проведения диагностики не требуется. Главное условие – не мочиться за несколько часов до процедуры. Желательно не вступать в половые контакты за 2-3 дня до обследования, а также не принимать алкоголь. При этом нельзя забывать о проведении процедур для поддержания интимной гигиены.
Как сдают анализ мужчины
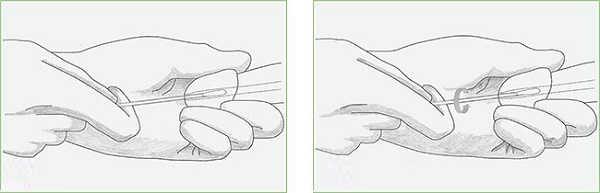 Головка полового органа вместе с мочеиспускательным каналом обрабатывается физ. раствором. Врач использует специальную щеточку, вставляемую примерно на 4 сантиметра. С помощью легкого вращения собирается материал для исследования с уретры. Полученный анализ оставляется в пробирке и отправляется на дальнейшее исследование в лабораторию. Биоматериал при этом может храниться не более 2 суток с момента получения.
Головка полового органа вместе с мочеиспускательным каналом обрабатывается физ. раствором. Врач использует специальную щеточку, вставляемую примерно на 4 сантиметра. С помощью легкого вращения собирается материал для исследования с уретры. Полученный анализ оставляется в пробирке и отправляется на дальнейшее исследование в лабораторию. Биоматериал при этом может храниться не более 2 суток с момента получения.
Как сдают анализ женщины
Перед взятием анализа на шейку матки наносят стерильный раствор. Затем с помощью щеточки берется мазок из цервикального канала. Приспособление оказывается на глубине около сантиметра, потом врач делает соскоб со стенок вращательными движениями. Биоматериал помещается в пробирку, где находится примерно 15 секунд. Там врач обтирает его об стенки, а затем вынимает. После этого содержимое пробирки отправляется на диагностику.
Забор биоматериала
Правильный забор материала – залог успешного проведения диагностики. Если при этом процессе нарушается стерильность, и в пробирку попадают чужеродные микроорганизмы, может произойти обнаружение «вируса», которого в действительности нет. Кроме того, ошибка может произойти из-за небольшого количества клеток, взятых на анализ.
Расшифровка анализа ПЦР
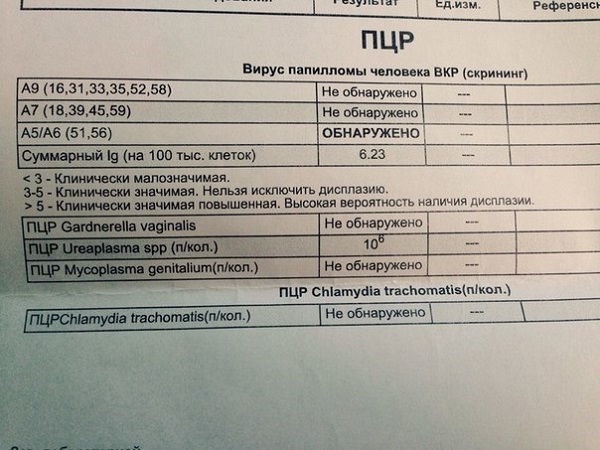
В зависимости от способа диагностики пациент увидит различные контрольные результаты. Графа «не обнаружено» свидетельствует о том, что вирус не присутствует в организме, либо его количество настолько незначительно, что не поддается обнаружению. Результат «обнаружено», соответственно, говорит о наличии патологического процесса.
Если пациент использовал количественный метод, расшифровка будет следующей:
- Lg 5 и выше – показатель большой концентрации вируса;
- Lg 3−5 – уровень вируса значительный, но не критический;
- Lg меньше 3 – малозначимое количество вирусных клеток.
В любом случае точной расшифровкой должен заниматься врач, ведь на основании этого ставится диагноз. Кроме того, через какое-то время желательно повторить процедуру, чтобы исключить ложноотрицательный или ложноположительный результат.
Источник
Исследование для выявления онкогенного вируса папилломы человека (ВПЧ) 16 типа, в ходе которого с помощью метода полимеразной цепной реакции в реальном времени (РТ-ПЦР) определяется генетический материал (ДНК) вируса в образце биоматериала.
Синонимы русские
Вирус папилломы человека, ВПЧ, 16 тип, папиллома-вирус.
Синонимы английские
HPV-16 [Real-Time Polymerase Chain Reaction, quantitative RT-PCR, qPCR, qRT-PCR], OncogenicHPV, High-riskHPV, hrHPV.
Метод исследования
Полимеразная цепная реакция с обратной транскрипцией в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Соскоб из прямой кишки, соскоб урогенитальный.
Общая информация об исследовании
В большинстве случаев рак шейки матки обусловлен инфекцией вирусом папилломы человека (ВПЧ). На сегодняшний день известно около 150 разновидностей ВПЧ, обладающих разной способностью к персистенции в эпителии шейки матки и разной степенью онкогенного риска. 16 тип ВПЧ относится к группе так называемых ВПЧ высокого онкогенного риска. Показано, что 50 % случаев рака шейки матки вызваны 16 типом ВПЧ. Также 16 тип ВПЧ может быть выявлен в подавляющем большинстве случаев рака вульвы, влагалища, ануса и полового члена. На сегодняшний день исследование РТ-ПЦР на ВПЧ 16 типа включено в программу скрининга рака шейки матки и предраковых состояний и наблюдения женщин с этими заболеваниями.
РТ-ПЦР является методом молекулярной диагностики, позволяющим выявлять в биологическом материале (например, в урогенитальном мазке) фрагменты генетического материала ДНК ВПЧ, а также производить количественную оценку вирусной нагрузки (в крестах).
Исследование РТ-ПЦР на ВПЧ рекомендуется в следующих ситуациях:
1. При выявлении в цитологическом мазке атипичных клеток плоского эпителия неясного значения;
2. При дальнейшем наблюдении женщин с патологическими признаками в цитологическом мазке, но нормальными результатами кольпоскопии/биопсии;
3. При оценке эффективности лечения ЦИН 2+ (дисплазия средней степени);
4. При проведении скрининга рака шейки матки и предраковых состояний в группе женщин старше 30 лет в сочетании с цитологическим мазком. Следует отметить, что на данный момент использование РТ-ПЦР в комбинации с цитологическим мазком рекомендовано только в группе женщин старше 30 лет. Использование РТ-ПЦР в качестве скринингового теста (отдельно или в комбинации с цитологическим мазком) в группе женщин младше 30 лет не рекомендовано. Также скрининг рака шейки матки не проводится в группе женщин старше 65 лет.
Традиционно для скрининга рака шейки матки используется цитологический мазок по Папаниколау. С помощью этого теста можно выявить наличие атипичных клеток и заподозрить предраковые изменения эпителия шейки матки на ранних стадиях (цервикальную интраэпителиальную неоплазию, ЦИН). При сравнении результатов скрининга с помощью цитологического мазка и исследования РТ-ПЦР было показано, что метод РТ-ПЦР позволяет выявлять женщин с диспластическими изменениями эпителия на более ранних стадиях. Метод РТ-ПЦР обладает очень высокой чувствительностью, превосходящей чувствительность цитологического мазка. Высокая чувствительность теста означает, что отрицательный результат на ВПЧ 16 в сочетании с отрицательным результатом исследования на другие онкогенные ВПЧ практически позволяет исключить риск развития рака шейки матки. Благодаря этому при использовании метода РТ-ПЦР в программе скрининга рака шейки матки интервал между повторными скрининговыми анализами может быть увеличен до 5 лет (по сравнению с 3 годами при использовании только цитологического мазка).
Метод РТ-ПЦР характеризуется очень высокой специфичностью и способен выявлять конкретный тип вируса. Это чрезвычайно важно, учитывая абсолютно разные подходы к ведению женщин с ВПЧ высокого и низкого онкогенного риска. Так, положительный результат на ВПЧ 16 типа свидетельствует о наличии именно 16 типа ВПЧ и будет отрицательным при наличии неонкогенных типов ВПЧ (например, 6 или 8). С другой стороны, опять же благодаря высокой специфичности, исследование РТ-ПЦР на ВПЧ 16 типа не дает никакой информации о наличии других типов ВПЧ высокого онкогенного риска, например ВПЧ 18.
Следует отметить, что специфичность РТ-ПЦР в отношении вируса и в отношении рака шейки матки – это не одно и то же. Действительно, специфичность теста в отношении вируса очень высокая. Однако из-за того, что многие, даже выраженные диспластические изменения эпителия шейки матки, связанные с ВПЧ, спонтанно и бесследно регрессируют, специфичность РТ-ПЦР в отношении рака шейки матки не такая высокая. Поэтому однократный положительный результат анализа РТ-ПЦР на ВПЧ-16 не всегда говорит о наличии риска рака шейки матки и предраковых состояний. Это особенно касается молодых женщин. С другой стороны, сохранение положительного результата РТ-ПЦР при повторных анализах на протяжении более 2 лет свидетельствует о высоком риске развития ЦИН высокой степени в ближайшие 5-10 лет.
Метод РТ-ПЦР не предназначен для скрининга злокачественных или предраковых заболеваний, вызванных ВПЧ 16 типа, у мужчин.
Следует отметить, что кроме 16 типа существует еще около 15 других типов ВПЧ высокого онкогенного риска. По этой причине отрицательный анализ РТ-ПЦР на ВПЧ 16 типа не позволяет полностью исключить риск рака шейки матки и должен быть дополнен другими лабораторными тестами.
Для чего используется исследование?
- Для скрининга рака шейки матки и предраковых состояний и наблюдения женщин с этими состояниями.
Когда назначается исследование?
- При выявлении в цитологическом мазке атипичных клеток плоского эпителия неясного значения (ACS-US);
- при дальнейшем наблюдении женщин с патологическими признаками в цитологическом мазке, но нормальными результатами кольпоскопии/биопсии;
- при оценке эффективности лечения ЦИН 2+;
- каждые 5 лет при проведении скрининга рака шейки матки и предраковых состояний в группе женщин 30-60 лет в сочетании с цитологическим мазком.
Что означают результаты?
Референсные значения: отрицательно.
Положительный результат:
- ВПЧ 16 типа (ВПЧ высокого онкогенного риска).
Отрицательный результат:
- норма;
- прекращение инфекции;
- неправильный сбор биоматериала для исследования.
Что может влиять на результат?
Наличие в образце биоматериала крови может препятствовать проведению реакции.
Важные замечания
- Однократный положительный результат анализа РТ-ПЦР на ВПЧ-16 не означает наличие риска рака шейки матки и предраковых состояний;
- отрицательный анализ РТ-ПЦР на ВПЧ 16 типа не позволяет полностью исключить риск рака шейки матки.
Также рекомендуется
[09-018] Human Papillomavirus 16/18 (HPV 16/18), ДНК [реал-тайм ПЦР]
[09-019] Human Papillomavirus 31/33 (HPV 31/33), ДНК [ПЦР]
[09-105] Human Papillomavirus высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы), ДНК без определения типа [реал-тайм ПЦР]
[09-106] Human Papillomavirus высокого канцерогенного риска (16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 типы), ДНК генотипирование [реал-тайм ПЦР]
[12-050] Цитологическое исследование мазков (соскобов) с поверхности шейки матки (наружного маточного зева) и цервикального канала – окрашивание по Папаниколау (Рар-тест)
Кто назначает исследование?
Гинеколог, врач общей практики.
Литература
- Poljak M, Oštrbenk A. The Abbott RealTime High Risk HPV test is a clinically validated human papillomavirus assay for triage in the referral population and use in primary cervical cancer screening in women 30 years and older: a review of validation studies. Acta Dermatovenerol Alp Panonica Adriat. 2013;22(2):43-7.
- Lowy DR, Solomon D, Hildesheim A, Schiller JT, Schiffman M. Human papillomavirus infection and the primary and secondary prevention of cervical cancer. Cancer. 2008 Oct 1;113(7 Suppl):1980-93. Review.
- U.S. Preventive Services Task Force. Screening for cervical cancer: recommendation statement. Am Fam Physician. 2012 Sep 15;86(6):555-9.
- Juckett G, Hartman-Adams H. Human papillomavirus: clinical manifestations and prevention. Am Fam Physician. 2010 Nov 15;82(10):1209-13.
Источник


