Онкомаркер на меланому в инвитро
Метод определения
Электрохемилюминесцентный иммуноанализ, Cobas e601(Roche).
Аналитическая чувствительность
Исследуемый материал
Сыворотка крови
Маркёр потенциального повреждения мозга, маркёр злокачественной меланомы.
Белки семейства S100 (к настоящему времени известно, по крайней мере, 25 представителей: S100A1 – S100A18, trichohylin, fillagrin, repetin, S100B, S100G, S100P, S100Z) – небольшие димерные кальцийсвязывающие белки с м.в. около 10,5 кДа, присутствующие только у позвоночных. S100 белки составляют самую большую подгруппу так называемых «EF-hand» кальцийсвязывающих белков (по структуре кальцийсвязывающего участка: спираль E – петля – спираль F), к которым, для примера, относятся также кальмодулин и тропонин С. Название S100 было дано при его первом описании по растворимости (solubility) в 100% насыщенном сульфате аммония. S100 белки могут формировать как гомо-, так и гетеродимеры, помимо Ca2+ связывать также Zn2+ и Сu2+.. Захват ионов меняет пространственную организацию S100 белка и обеспечивает возможность связи с различными белками – мишенями их биологического действия (документировано более 90 потенциальных белков-мишеней).
Представители S100 белков демонстрируют выраженную тканеспецифичную и клеточноспецифичную экспрессию. Они вовлечены в различные процессы – сокращение, подвижность, клеточный рост и дифференциация, прогрессия клеточного цикла, транскрипция, клеточная организация мембран и динамика цитоскелета, защита от оксидативного повреждения клетки, фосфорилирование, секреция. Предполагается, что S100 белки выполняют как внутриклеточные, так и внеклеточные функции, некоторые S100 белки секретируются и действуют аналогично цитокинам. S100Β, который продуцируется преимущественно астроцитами мозга, является маркёром активации астроглии, опосредующим свои эффекты через взаимодействие с RAGE (receptor for advanced glycation end products – рецепторы конечных продуктов гликозилирования). Показано, что S100Β проявляет нейротрофическую активность при физиологической концентрации и нейротоксическую при высокой концентрации. Различные формы рака проявляют выраженное изменение продукции S100. Повышенная секреция S100Β характерна для злокачественной меланомы. S100 – RAGE взаимодействие играет важную роль в связи воспаления и рака, выживании опухолевых клеток и злокачественной прогрессии. Клинический интерес к S100 связан с применением его как маркёра повреждения мозга при травматических поражениях мозга, болезни Альцгеймера (S100Β, высвобождающийся из некротических тканей может усиливать нейродегенерацию путём S100Β-индуцированного апоптоза), субарахноидальных кровотечениях, инсультах и иных неврологических расстройствах; в мониторинге злокачественной меланомы, других неопластических заболеваний, а также воспалительных болезнях.
Представляемый Независимой лабораторий ИНВИТРО тест количественного определения S100 (COBAS, Roche Elecsys 1010) направлен на выявление димеров S100A1B и S100BB. S100A1 и S100B (функциональные белки могут быть представлены как гомо- так и гетеродимерами) преимущественно экспрессируются клетками центральной нервной системы, главным образом, астроглией, но также продуцируются и в клетках меланомы и, в некоторой степени, в других тканях. Тест можно использовать для мониторинга и контроля лечения, раннего выявления метастазов и рецидивов (но не для постановки диагноза!) у пациентов со злокачественной меланомой и в целях комплексной оценки состояния пациентов с предполагаемым повреждением мозга.
Меланома. Секреция S100 повышена у пациентов, страдающих от злокачественной меланомы (особенно, в стадиях II, III и IV), уровень S100 коррелирует с прогрессией опухоли, стадией заболевания и может использоваться в целях прогноза, выявления рецидивов и метастазов (не для первичного диагноза). Превышение пороговой величины теста при мониторировании лечения пациентов с меланомой можно ожидать, в среднем, в % – у пациентов без проявлений заболевания – в 5,5%; с региональными метастазами – в 12,5%; метастазами в коже/дистантных лимфоузлах – в 47,6%; дистантными/висцеральными метастазами – в 42,9% (по результатам последующего наблюдения). В контрольной группе здоровых людей превышение порога наблюдается у 4,9% (доверительный интервал 95%).
В случае выявления повышенного уровня S100 рекомендован повтор исследования в целях исключения ложноположительного результата и проведение соответствующих томографических исследований для повышения точности диагностики.
Взрослые пациенты с потенциальным повреждением мозга. Уровень S100 растёт в спинномозговой жидкости и высвобождается в кровь при различных клинических ситуациях. Измерение S100 при неврологических нарушениях сравнивают c измерением СРБ при системном воспалении. S100 может быть обнаружен у пациентов с повреждениями мозга разного происхождения, включая травматические повреждения или инсульт.
После инсульта рост S100 начинается в период первых 8 часов, повышение сохраняется в течение 72 часов, концентрация S100 коррелирует с объемом повреждения и неврологическими последствиями инсульта. Повышение S100 после спонтанных субарахноидальных кровотечений коррелирует с тяжестью патологии (уровень выше 0,3 мкг/л ассоциирован с неблагоприятным течением). Травматические повреждения мозга сопровождаются ростом уровня S100 в спинномозговой жидкости и сыворотке.
При сопоставлении концентрации S100 с результатами томографии продемонстрирована высокая отрицательная предсказательная ценность теста (отсутствие повреждения по результатам томографии при отрицительном результате S100) – 99 – 100%, но низкая позитивная предсказательная ценность (наличие повреждений мозга по томограмме при результатах S100 выше порога) – 9 – 13%. Чувствительность теста 96,5 – 100%, специфичность 30 – 35% при доверительном интервале 95%. При умеренных травматических повреждениях мозга рост S100A1B и S100BB может наблюдаться у 31% и 48% пациентов без заметных признаков когнитивных расстройств. Показатель нельзя рассматривать как достоверное предсказание длительных неврологических исходов в таких случаях, особенно у детей.
Следует осторожно интерпретировать результаты, учитывая возможность влияния изменения целостности гематоэнцефалического барьера. Раннее высвобождение S100 может быть следствием механического выделения при повреждении гематологического барьера или активации экспрессии S100B при вовлечении мозга в системную воспалительную реакцию. Потенциально возможны внемозговые источники S100B (хондроциты, адипоциты). Рост S100 (>1,5 мкг/л) после остановки сердца и последующей реанимации отражает высокий риск тяжёлых неврологических последствий.
Предпочтительно выдержать 4 часа после последнего приема пищи, обязательных требований нет.
С общими рекомендациями для подготовки к исследованиям можно ознакомиться
здесь >>
.
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Обращаем внимание! Измерение концентрации S100 может значительно варьировать в зависимости от процедуры тестирования, результаты, полученные разными методами нельзя прямо сравнивать друг с другом, это может послужить причиной неверной интерпретации. При необходимости смены процедуры тестирования S100 в ходе серийного мониторинга сопоставимость результатов должна быть подтверждена параллельным измерением двумя методами.
Единицы измерения в Независимой лаборатории ИНВИТРО: мкг/л.
Референсные значения:
метаболические повреждения мозга;
травматические повреждения мозга;
спонтанные субарахноидальные кровотечения;
болезнь Альцгеймера;
инсульт;
множественный склероз (колебания уровня);
системная красная волчанка (с нейропсихиатрическим вовлечением – органический мозговой синдром, судороги, сосудистые инциденты, психоз);
печёночная энцефалопатия;
биполярные расстройства в период обострений, но не в период ремиссий;
неврологические нарушения после остановки сердца и последующей реанимации;
физиологические условия: интенсивные физические тренировки.
Источник
Метод определения
Гистологическое исследование биоптата кожи (опухолевого очага) (окрашивание гематоксилин-эозином) с морфологической оценкой опухоли согласно гистологической классификации ВОЗ, оценкой глубины инвазии по шкале Кларка и Бреслоу.
Иммуногистохимическое исследование с применением антител к протеину S-100, Melan A, HMB-45, SOX-10 (пероксидазный и авидин-биотиновый методы).
Исследуемый материал
Парафиновый блок с биоптатом кожи (опухолевого очага)
Меланоцитарные опухоли кожи представляют собой гетерогенную группу доброкачественных и злокачественных новообразований со специфическими клиническими, морфологическими и генетическими признаками. Клинически и с точки зрения здравоохранения, злокачественные меланомы являются значимой группой злокачественных опухолей кожи в связи с высокой тенденцией к лимфогенному и гематогенному метастазированию. Частота меланом составляет 1,8-2,2 на 100 тыс. населения и 1% от числа всех злокачественных новообразований. Меланомы возникают у женщин гораздо чаще, чем у мужчин.
В 50-е и 60-е годы ХХ века считалось, что при обнаружении меланомы пациент имеет плохой прогноз, но с середины 1970-х годов выживаемость при этом заболевании в развитых странах значительно возросла. Это связано не только с ранней диагностикой, но и с программой Всемирной организации здравоохранения (ВОЗ) по первичной и вторичной профилактике заболевания.
Преимущественной локализацией меланомы у женщин являются нижние конечности (голень), у мужчин – туловище (чаще спина); у лиц обоих полов старшей возрастной группы (65 лет и старше) меланома локализуется преимущественно на коже лица. В значительном большинстве случаев (примерно у 70% пациентов) меланома развивается на месте врожденных или приобретенных невусов, и только у 28-30% – на неизмененной коже (melanoma cutis de novo).
При подозрении на меланому обязательно проводят биопсию пораженного очага с последующим гистологическим исследованием, оценкой краев резекции опухоли. Определяющим в диагностике является морфологическое исследование удаленного очага с последующим иммуногистохимическим исследованием.
В дифференциальной диагностике меланомы принято использовать ИГХ исследование биоптатов для оценки экспрессии панели маркеров, которые в комплексном применении обеспечивают максимальную чувствительность и специфичность иммуноморфологического исследования. Такой комплекс маркеров чаще включает протеин S-100, Melan А (MART-1), HMB-45, SOX-10, а также некоторые другие.
Протеин S-100 впервые был идентифицирован в 1965 г. B.W. Moore и получил свое название благодаря растворимости в 100% насыщенном растворе сульфата аммония. Относится к группе кальций связывающих белков с молекулярной массой 21 кДа, которые участвуют в клеточном цикле, дифференцировке, в процессах взаимодействия цитоскелета с мембраной, выполняют как внутриклеточные, так и внеклеточные функции. Экспрессируется шванновскими клетками периферической нервной системы, гистиоцитами с антиген-презентирующей функцией типа клеток Лангерганса, адипоцитами, хондроцитами, меланоцитами, миоэпителиальными клетками, клетками мозгового вещества надпочечников, фолликулярными дендритными клетками. Протеин S-100 локализуется в клеточной мембране, цитоплазме, ядре. С диагностической точки зрения, белок S-100 рассматривается как чувствительный, но неспецифический маркер меланоцитов (может выявляться в клетках других опухолей: липосарком, хондросарком, шванном и пр.), в дифференциальной диагностике экспрессия протеина S-100 используется в панели с другими маркерами меланомы. Ген Меlan A/MART-1 (Melanoma Antigen Recognized by T-cells 1) кодирует белок с молекулярной массой 20-22 кДа, связанный с эндоплазматическим ретикулумом и премеланосомами, распознаваемый Т-лимфоцитами. Гликопротеин Меlan A/MART-1 локализуется на внутренней мембране премеланосом 1, 2, 3-го типов. Меlan A/MART-1 является более специфичным маркером, чем белок S-100, поэтому его включают в стандартную панель для типирования меланом.
HMB-45 (Melanosome) – специфический меланосомный антиген (Melanosome Specific Antigen, MSA), который взаимодействует с чувствительной к нейроаминидазе олигосахаридной боковой цепью гликоконъюгата. Кодирует белок GP100 с молекулярной массой 10 кДа, который локализуется на внутренней мембране премеланосом 1, 2, 3-го типов, обнаруженный моноклональным антителом HMB-45. Он является высокоспецифичным маркером меланоцитарной дифференцировки, однако HMB-45 менее чувствителен, чем Меlan A.
SOX-10 (member of the sex-determining region Y-related HMG-box family) – белок, кодируемый геном на 22-й хромосоме (22q13.1), является ядерно-транскрипционным фактором, участвующим в регуляции миграции клеток нервного гребня на этапах эмбриогенеза, в дифференцировке клеток меланоцитарной линии. Экспрессия ядерного белка SOX-10 сохраняется в клетках с признаками глиальной и шванновской дифференцировки, миоэпителиальных клетках слюнных, бронхиальных, эккриновых и молочных желез, а также наблюдается в тучных клетках различных тканей и органов, как в ядре, так и в цитоплазме. Исследованиями последних лет показано, что SOX-10 является более специфичным и чувствительным маркером меланом обычного, веретенообразного и десмопластического подтипов по сравнению с протеином S-100. Рутинно используемые маркеры меланомы HMB-45 и Меlan A/MART-1 в десмопластической меланоме выявляются в 10% случаев, в то время как чувствительность и специфичность SOX-10 для определения десмопластической меланомы составляет до 98%.
В ряде случаев дополнительно проводится определение экспрессии следующих маркеров:
MiTF (Microphthalmia-associated Transcription Factor) – известного, как основной белок класса E спирали петли спирали 32 или bHLHe32, кодируемый геном MITF. Член семейства транскрипционных факторов микрофтальмии, регулирующих гены, которые кодируют ферменты меланогенеза. Является ведущим регуляторным меланоцитарным ядерным белком, регулирующим экспрессию белков: тирозиназы и связанного с тирозиназой белка TYRP1 (Tyrosinase-related protein 1), а также MART-1, GP-100. Высокая экспрессия MiTF наблюдается в 81-100% меланом, однако экспрессия часто отрицательна в вариантах из десмопластических и веретенообразных клеток.
PNL2 (Melanoma Associated Antigen) – белок, присутствующий в цитоплазме активированных меланоцитов и меланоцитарных опухолей. Антитела к PNL2 обладают высокой чувствительностью для выявления метастатической меланомы (87%), в отличие от антител к НМВ-45 (76%) и антител к MART-1 (82%). Используется для выявления внутриэпидермальных невусов, в то время как дермальный компонент сложных невусов не реагирует с антителами к PNL2.
Литература
- Ахмедова А.А., Шихлярова А.И., Шейко Е.А., Сустретов В.А. Меланома: Некоторые современные аспекты развития и диагностики. Современные проблемы науки и образования. 2017;5;181. https://www.science-education.ru/ru/article/view?id=27024
- Гилязутдинов И.А., Хасанов Р.Ш., Сафин И.Р., Моисеев В.Н. Злокачественные опухоли мягких тканей и меланома кожи. – М.: Изд. «Практическая Медицина». 2010:204.
- Клинические рекомендации. Меланома кожи. Ассоциация онкологов России. Ассоциация специалистов по проблемам меланомы. 2017:77. https://oncology-association.ru/docs/melanoma_kozhi_2017.pdf
- Лезвинская Е.М., Вавилов А.М. Лимфопролиферативные опухоли кожи. – СПб.: Изд. «Практическая Медицина». 2010:368.
- Новик А.В. Практическая онкология. 2011;12(1):185.
- Червонная Л.В. Пигментные опухоли кожи. – СПб.: Изд. «ГЭОТАР-Медиа». 2014:224.
- Bloethner S., Scherer D., Drechsel M. et al. Malignant melanoma – a genetic overview. Actas dermo-sifiliográficas. 2009;100(1):3851.
- Hersey P., Smalley K.S., Weeraratna A. et al. Meeting report from the 7th International Melanoma Congress, Sydney, November, 2010. Pigment cell and melanoma research. 2011;24(1):15.
- Hoek K.S., Goding C.R. Cancer stem cells versus phenotypeswitching in melanoma. Pigment cell and melanoma research. 2010;23(6):746759.
- Kyrgidis A., Tzellos T.G., Triaridis S. Melanoma: Stem cells, sun exposure and hallmarks for carcinogenesis, molecular concepts and future clinical implications. Journal of carcinogenesis. 2010;9(3):115.
- Mueller D.W., Bosserhoff A.K. Role of miRNAs in the progression of malignant melanoma. British journal of cancer. 2009;101(4):551556.
- Palmieri G., Capone M., Ascierto M.L. et al. Main roads to melanoma. Journal of translational medicine. 2009;7(86):16.
- Spatz A., Stock N., Batist G. et al. The biology of melanoma prognostic factors. Discov. Med. 2010;10(50.):87.
- Dabbs D.J. Diagnostic Immunohistochemistry: Theranostic and Genomic Applications. Elsevier, 4-th Edition. 2013:960.
Источник
07.12.2017
Две истории сподвигли меня написать статью об онкомаркерах.
1) Недавно мне в соцсети «ВКонтакте» пришло вот такое очень тревожное сообщение:
«Здравствуйте, Дмитрий Сергеевич! Подскажите, пожалуйста, успокоится не могу, вся на нервах. Дерматолог нашел подозрительное пятно на виске и назначил онкомаркер s-100. Он оказался увеличен достаточно сильно. При визуальном осмотре онколог ничего не увидел – как быть? Что теперь дальше делать? У меня просто двое грудничков на руках. Спасибо Вам за ответ, очень благодарна!»
2) Увидел на You Tube рекламный ролик клиники одного из городов с миллионным населением. Врач-онколог (!!!) высшей категории (!!!) перед удалением родинки рекомендует сдать онкомаркеры S-100 и SCC, чтобы «убедиться, что удаляемая родинка доброкачественная». Причем делает это не втихаря, чтобы никто, кроме пациента не услышал, а на You Tube.
Пришло время разобраться с онкомаркерами – что это, зачем они нужны и какую реальную диагностическую ценность представляют.
Речь, естественно, пойдет об онкомаркерах при злокачественных опухолях кожи.

Уровень онкомаркеров измеряется при анализе крови
Что такое S-100?
S-100 – это белок, вернее целое семейство белков, которые участвуют в самых различных процессах в организме. Именно их клетки меланомы могут выделять в кровь. И именно их уровень можно измерить, на основании чего сделать предположения о диагнозе «меланома».
К сожалению, уровень этого белка может быть повышен не только при меланоме, но и при других опухолях – при раке молочной железы, яичников, желудка, простаты и некоторых других.
Еще одна особенность, которую нужно знать: уровень S-100 может повышаться при ревматиодном артрите, субарахноидальном кровоизлиянии, острой ишемии миокарда, псориазе и др.
Насколько ценен S-100 в диагностике меланомы?
Существуют как минимум два исследования, в которых показано, что диагностическая ценность S-100 при диагностике меланомы на ранних стадиях очень низкая.
Скажу прямо – никакая.
При I–II стадии меланомы уровень S-100 повышен у 1,3 % больных, при III стадии – у 8,7 % и только при IV стадии этот белок повышается у 73 % пациентов. Другими словами, даже на IV стадии меланомы S-100 может не показать, что у человека есть это заболевание.
Все авторы отмечают, что уровень S-100 в качестве диагностического теста не обладает необходимой точностью для диагностики ранних стадий меланомы.

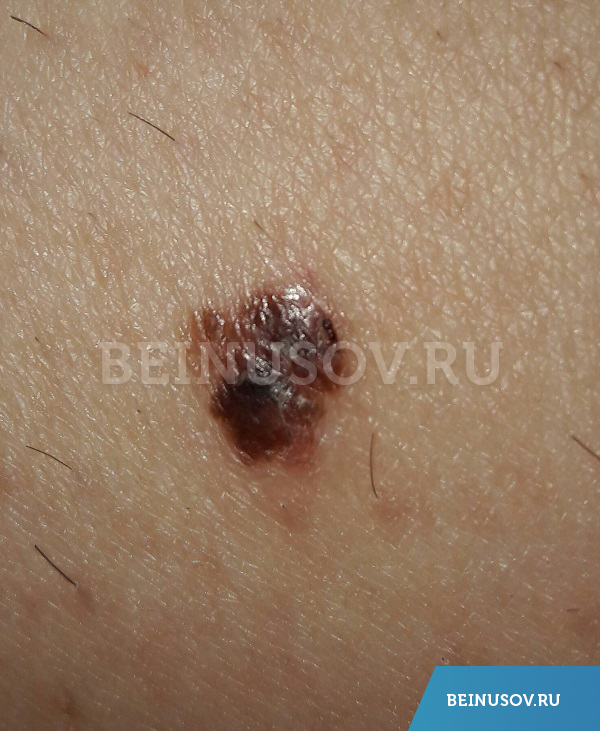
Меланома кожи
Что такое ЛДГ?
ЛДГ (лактатдегидрогеназа) – фермент, т. е. особое вещество, которое участвует в цикле превращения глюкозы в энергетические молекулы АТФ.
Уровень этого вещества в крови чаще всего повышен в ситуации, когда в организме уже есть регионарные или отдаленные метастазы меланомы. В настоящее время мне не удалось найти исследования, в которых отмечено, что данный фермент может быть использован для диагностики этой опухоли на ранних стадиях.
Что такое SCCA (squamous cell carcinoma antigen)?
SCC антиген – специфический белок, который могут выделять клетки плоскоклеточного рака слизистых и кожи. К сожалению, с его диагностической ценностью абсолютно та же беда, что и у S-100.
Уровень SCC антигена по данным исследований повышается только у 44 % больных плоскоклеточным раком кожи или слизистых. Кроме этого, повышенные значения SCC могут также быть при псориазе, экземе, атопическом дерматите, почечной недостаточности, туберкулезе, саркоидозе, а также при раке пищевода, легкого, анального канала и вульвы.
Эти факты говорят о том, что для диагностики первичной опухоли при плоскоклеточном раке кожи SCC не может и не должен применяться.
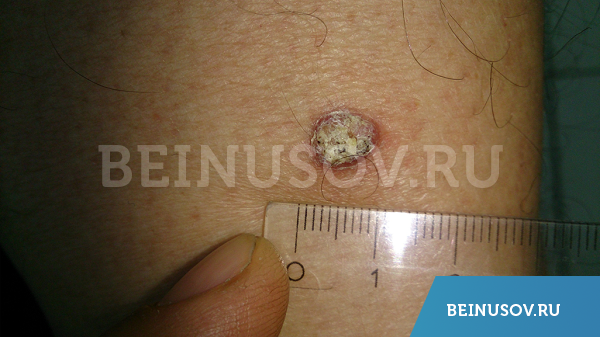
Плоскоклеточный рак кожи
Какое реальное практическое применение имеют S-100, ЛДГ и SCCA сейчас?
Все 3 указанных маркера могут быть использованы для трех целей:
1) Контроль за прогрессированием заболевания – развитием метастазов и рецидивов.
2) Наблюдение за ответом на проводимую терапию.
В ситуациях 1) и 2) важно знать уровни S-100 и ЛДГ, которые были до лечения.
3) Как отдельные прогностические факторы. Причем в случае с меланомой это верно больше для ЛДГ, чем для S-100. Для SCC при плоскоклеточном раке кожи и слизистых это утверждение, мягко говоря, не доказано.
Какой тест наиболее точен для диагностики меланомы и рака кожи?
Наиболее точный диагностический тест при подозрении на меланому и рак кожи – эксцизионная биопсия (полное удаление) образования целиком с захватом 1–3 мм здоровой кожи и с последующим гистологическим исследованием. В некоторых случаях возможно удаление фрагмента (инцизионная биопсия) подозрительного образования с захватом наиболее толстой части, также с гистологией.
Обратите внимание – это не мое мнение. Так считают крупные онкологические ассоциации NCCN и ESMO. Ни о каком цитологическом исследовании соскобов, пункций родинок или дерматоскопии нет ни слова в их практических рекомендациях – это вспомогательные предварительные тесты.
Почему нельзя сдавать онкомаркеры «просто так для профилактики»?
Потому что результат этих тестов при необоснованном назначении очень часто может быть недостоверным. Есть 2 варианта:
1) Ложноположительный результат – тест говорит, что рак есть, а его на самом деле нет. Человек начинает судорожно обследоваться, ничего нигде не находят, и развивается самый настоящий невроз.
2) Ложноотрицательный – тест говорит, что рака нет, а он есть. Здесь еще хуже: вместо адекватных обследований человек успокаивается и выращивает опухоль до поздних стадий, когда лечение уже малоэффективно.
Что делать, если сдали онкомаркеры S-100, SCC и они положительные?
К сожалению, нужно будет достаточно углубленно обследоваться, иначе расслабиться, скорее всего, уже не получится. Необходимы ПОЛНЫЙ осмотр всей кожи у онколога-дерматолога с проведением дерматоскопии всех родинок на теле, клинический и биохимический анализы крови, мочи, УЗИ брюшной полости и всех групп лимфатических узлов, малого таза, рентгенография органов грудной клетки.
При обнаружении положительных онкомаркеров потребуется провести полную диагностику
Нужно ли сдавать онкомаркеры после удаления родинки без гистологии?
Нет, это бессмысленно, т. к. даже при наличии меланомы на I–III стадии они не информативны.
Резюме, или Коротко о главном
Онкомаркеры при первичной диагностике меланомы и рака кожи бесполезны.
Более того, сдавать их в качестве единственного метода обследования настоятельно не рекомендую, т. к. при ложно-положительном результате может развиться невроз. Онкомаркеры S-100, ЛДГ и SCCA в настоящее время очень ограниченно применяются в дерматоонкологии.

Другие статьи:
- Частые вопросы: что можно и что нельзя делать перед и после удаления родинки
- Бритье, эпиляция и татуировки при наличии родинок
- Почему важно выявить меланому на ранней стадии
- Много родинок на теле – это сколько?
Полезная статья? Сделайте репост в Вашей социальной сети!
Оставьте комментарий или задайте вопрос
Источник

