Что такое впч инфекция и cin
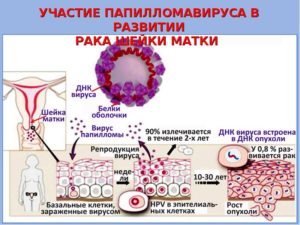
ДИСПЛАЗИЯ ШЕЙКИ МАТКИ – ЭТО ПРЕДРАКОВЫЙ ПРОЦЕСС, ХАРАКТЕРИЗУЮЩИЙСЯ НАРУШЕНИЕМ СОЗРЕВАНИЯ МНОГОСЛОЙНОГО ПЛОСКОГО ЭПИТЕЛИЯ В РЕЗУЛЬТАТЕ ДЛИТЕЛЬНОЙ ПЕРСИСТЕНЦИИ ВИРУСА ПАПИЛЛОМЫ ЧЕЛОВЕКА.
Синонимы: цервикальная интраэпителиальная неоплазия (CIN), плоскоклеточное интраэпителиальное поражение (SIL).
Если коротко, дисплазия шейки матки — это заболевание, которое в будущем может привести к раку. Вероятность этого тем выше, чем выше степень дисплазии. К дисплазии 1 степени (CIN 1, LSIL) относят любые изменения эпителия, порой даже минимальные и субъективные. Это позволяет взять женщину под контроль и не допустить прогрессирования процесса. На практике, для диагностики дисплазии 1 степени достаточно поражение эпителиальных клеток вирусом папилломы человека. Опасаться этого не стоит! Легкая степень дисплазии самостоятельно проходит у 70% женщин в течение нескольких лет. За это время собственная иммунная система уничтожает вирус и заболевание регрессирует. Обычно дисплазия 1 степени требует только наблюдения, в части случаев может назначаться прижигание. Дисплазия 2 и 3 степени (CIN 2-3, HSIL) — это уже предопухолевый процесс с высоким риском, поэтому требует серьезного лечения. В таких случаях показана широкая эксцизия или конизация шейки матки. Диагностировать дисплазию эпителия можно с помощью мазка на цитологию или биопсии. В принятии решения и тактике лечения важную роль играет тест на ВПЧ.
Подробнее читайте ниже, а также посмотрите комментарии, там Вы найдете ответы на свои вопросы.
Содержание:
- Что такое дисплазия шейки матки? Причины
- Степени дисплазии и терминология (CIN 1, CIN 2, CIN 3, LSIL, HSIL)
- Диагностика дисплазии шейки матки: кольпоскопия, цитология и гистология. Что важнее?
- Нужен ли тест на ВПЧ?
- Лечение дисплазии шейки матки 1,2,3 степени
- Консультация online в комментариях
Основной причиной развития дисплазии шейки матки является вирус папилломы человека, а именно его онкогенные штаммы — 14 серотипов, среди которых наиболее важными являются 16 и 18. Зрелый многослойный плоский эпителий, покрывая наружную часть шейки, создает непреодолимую преграду для вируса. Единственным же уязвимым местом является граница с железистым эпителием у наружного зева, называемая зоной трансформации. При эрозии (эктопии) шейки матки зона трансформации смещается на наружную часть шейки матки, что создает предпосылки для инфицирования.
Более 80% случаев дисплазии и рака шейки матки развивается именно в зоне трансформации.
Большинство женщин переносит ВПЧ-инфекцию без каких либо изменений со стороны организма. В течение нескольких лет иммунная система самостоятельно избавляется от вируса. Однако 10% женщин не могут уничтожить вирус, который в свою очередь встраивается в ДНК эпителиальных клеток и модифицирует их, приводя к опухолевой трансформации. Это может быть связано как с индивидуальной предрасположенностью, так и с иммунодефицитом или длительными стрессами. Также известно, что курение способствует снижению специфического иммунитета против ВПЧ.
Дисплазия шейки матки — это качественное изменение клеток плоского эпителия, которое указывает на возможное начало опухолевой трансформации.
Степени дисплазии шейки матки и терминология (CIN, LSIL, HSIL)
Различают несколько степеней дисплазии шейки матки по тяжести, что обычно выражается в числовых значениях от 1 до 3. Каждая степень отражает прогноз патологического процесса и позволяет выбрать соответствующий алгоритм лечения. Так, дисплазия 1 степени имеет низкий потенциал к малигнизации и в большинстве случаев самостоятельно регрессирует в течение нескольких лет без какого-либо вмешательства. В противоположность, дисплазия 3 степени в течение одного года обязательно трансформируется в рак и требует уже специализированного хирургического лечения.

Прогрессирование дисплазии шейки матки
В международной практике термин “дисплазия шейки матки” имеет различные синонимы. Наиболее широко распространена аббревиатура CIN – цервикальная интраэпителиальная неоплазия, что означает развитие неоплазии (новообразования) в пределах эпителиального пласта. В отличие от рака, CIN не обладает способностью к инвазивному росту и метастазированию. На этом этапе можно предотвратить развитие злокачественной опухоли.
В 1988 г. была создана новая терминология — «SIL» (squamous intraepithelial lesion), что означает «плоскоклеточное интраэпителиальное поражение». Специалисты отказались от некорректного при данной патологии слова «неоплазия» и заменили его на «поражение». Степени тяжести процесса выделили всего две: легкую LSIL и тяжелую HSIL:
1) LSIL (low grade squamous intraepithelial lesion) — плоскоклеточное интраэпителиальное поражение легкой степени. LSIL соответствует CIN 1 или дисплазии 1 степени.
2) HSIL (hight grade squamous intraepithelial lesion) — плоскоклеточное интраэпителиальное поражение тяжелой степени, что соответствует CIN 2 и CIN 3. Умеренная и тяжелая дисплазия объединены в одну категорию, поскольку требуют одинакового подхода к лечению, а различия в некоторых случаях достаточно субъективны. Термин «рак in situ» сейчас практически не используется, по новой классификации отнесен в группу тяжелых интраэпителиальных поражений плоского эпителия.
| Pap class System 1954 | Классификация ВОЗ 1956 | Классификация Bethesda 1988 |
| Class | Дисплазия/CIN (ЦИН — цервикальная интраэпителиальная неоплазия) | SIL (плоскоклеточное интраэпителиальное поражение) |
| Class 3 | Дисплазия 1 степени/CIN 1 | LSIL — плоскоклеточное интраэпителиальное поражение легкой степени |
| Class 4 | Дисплазия 2 степени/CIN 2 | HSIL — плоскоклеточное интраэпителиальное поражение тяжелой степени |
| Дисплазия 3 степени/CIN 3 | ||
| Рак in situ (рак в пределах эпителиального пласта, без инвазивного роста) |
Диагностика
1. Мазок на цитологию

Первым методом в диагностике дисплазии шейки матки чаще всего является мазок на онкоцитологию. Это скрининговый метод для обследования большого количества женщин. Является самым простым и безопасным для женщины, однако не самым точным. Чувствительность метода составляет 60-70%, и только трехкратное исследование позволяет с высокой точностью определить или опровергнуть дисплазию эпителия. Кроме этого у молодых женщин часто бывают ложно-отрицательные результаты, когда дисплазия может быть пропущена; а у пожилых женщин часты ложно-положительные результаты, когда мазок показывает наличие дисплазии, в то время как более качественные методы ее исключают.
При определении LSIL в мазке необходимо только лишь активное наблюдение. Под этим диагнозом подразумеваются клеточные изменения с низким потенциалом опухолевой трансформации. К LSIL относятся различные дегенеративные изменения клеток при раздражении, воспалении или вирусном поражении. Гинеколог, получив такое заключение может порекомендовать проведение кольпоскопии с последующей точечной биопсией.
При наличии HSIL в мазке на цитологию проведение кольпоскопии с гистологическим подтверждением становится обязательным!
2. Кольпоскопия
Кольпоскопия — это метод осмотра наружной поверхности шейки матки с помощью специального микроскопа. Кольпоскопия является достаточно субъективным методом диагностики, сильно зависящим от опыта и умения врача. Кольпоскопические картины дисплазии шейки матки размыты и очень часто ее можно спутать с банальными физиологическими процессами, такими как плоскоклеточная метаплазия, вирусным поражением или лейкоплакией. Несмотря на это, кольпоскопия позволяет определить подозрительные места на шейке матки и взять биопсию — участок ткани для дальнейшего гистологического исследования.
К кольпоскопическим признакам дисплазии относятся: ацетобелый эпителий, йод-негативные зоны, изъеденность или нерегулярность эпителиального покрова, атипичные сосуды, мозаика, пунктация, контактная кровоточивость и др. Гинеколог должен оценить не только степень, но и скорость наступления тканевой и сосудистой реакции при обработке уксусной кислотой или йодом.
Цель кольпоскопии — это определить анатомическую локализацию зоны трансформации, что имеет решающее значение для дальнейшей тактики диагностики и лечения.
3. Биопсия
Биопсия является “золотым” стандартом диагностики дисплазии и рака шейки матки. Гистологическое исследование позволяет определить качество плоского эпителия и степень его созревания. Биопсия может быть точечной, получаемой с помощью специального инструмента — конхотома, или широкой (эксцизионной), получаемой с помощью электропетли.
Изменения при дисплазии 1 степени обычно носят характер цитопатического действия вируса папилломы человека. В эту категорию так же относят остроконечную и плоскую кондиломы. Морфологические изменения при CIN 1 (LSIL) включают: нарушение стратификации плоского эпителия преимущественно в базальных отделах, нарушение поляризации клеток относительно базальной мембраны, единичные делящиеся клетки, незначительный дискариоз, а также признаки вирусного поражения — койлоцитарную атипию в поверхностных отделах эпителия, дискератоз, пара- и гиперкератоз эпителия.

Патологическая эпидермизация желез с CIN III
Морфологические изменения при CIN 2-3 (HSIL) носят уже неопластический характер, а цитопатическое действие вируса может проявляться слабо. Нарастает клеточная атипия, которая затрагивает весь пласт плоского эпителия с минимальными признаками созревания. Клетки активно делятся, замещая нормальный эпителий цервикальных желез, в ряде случаев пролиферирующий плоский эпителий может замещать выстилку цервикального канала. Характерно обилие как нормальных, так и патологических митозов.
Тяжелая дисплазия шейки матки отличается от рака отсутствием инвазивного роста.
Нужен ли тест на ВПЧ?
Тест на ВПЧ помогает в диагностике дисплазии шейки матки и выборе тактики лечения в сложных ситуациях.
ВПЧ тест рекомендуется делать женщинам после 25 лет, поскольку имеется большая вероятность, что инфекция уже длительное время персистирует в организме и могла вызвать какие-либо изменения в шейке. В более молодом возрасте при нормальном мазке на цитологию ВПЧ-тистирование не дает полезной информации.
С возрастом ВПЧ-тестирование приобретает все большую значимость. К примеру, при наличии 16 или 18 штаммов ВПЧ у 50 летней женщины можно с высокой вероятностью утверждать, что у нее уже имеется тяжелое интраэпителиальное поражение эпителия. Мазок на цитологию менее эффективен в данном случае. Женщине тот час может рекомендоваться диагностическая биопсия и выскабливание цервикального канала.
Лечение дисплазии шейки матки
Тактика лечения и ведения пациенток с дисплазией зависит от гистологического заключения, кольпоскопической картины, типа зоны трансформации, возраста и планирования беременности. Основными методами являются абляция (прижигание), или эксцизия (удаление тканей). Эти методы могут проводиться с помощью различных инструментов, использующих низкие или высокие температуры, электро-, лазеро- или радиоволновую энергию.
Лечение LSIL (CIN 1):
По западным протоколам LSIL необходимо динамически наблюдать. Так как LSIL обладает низким злокачественным потенциалом и часто регрессирует самостоятельно, женщине рекомендуется проходить цитологическое исследование не менее 2 раз в год. В отечественной медицине часто рекомендуют абляцию (прижигание), хотя это не всегда оправдано. С прижиганием связывают некоторое повышение риска невынашивания беременности. Однако, часть авторов, опровергает это.
Наиболее оптимальным является радиоволновая абляция Сургитроном. Патологический эпителий и подлежащая строма выпариваются радиоволнами, после чего пораженная зона эпителизируется заново. Минусом абляции является отсутствие материала для последующего гистологического исследования, плюсом — сохранение анатомического строения шейки матки и небольшое количество осложнений.
Лечение HSIL (CIN 2, CIN 3):
HSIL обладает высоким злокачественным потенциалом, поэтому в данном случае показано удаление патологически изменненых тканей. Обычно, рекомендуется широкая эксцизионная биопсия или конизация шейки матки — это конусообразное удаление тканей, включающая наружную часть шейки матки и ткани вокруг цервикального канала. Весь удаленный материал отправляется на гистологическое исследование для подтверждения и уточнения диагноза. В удаленном материале гистолог оценивает края резекции, так как важно, чтобы патологический эпителий был удален в пределах здоровых тканей. При наличии в краях резекции патологии, или глубоком поражении цервикального канала, а также наличии инвазивного роста может быть принято решение об ампутации шейки матки.
Изредка, если женщина молода и планирует беременность, допускается лечение HSIL абляцией. Это возможно только лишь в случае 1 или 2 типа зоны трансформации при кольпоскопии, когда гинеколог видит глазом все измененные ткани и может обеспечить полную их абляцию. Если зона трансформации смещена глубоко в цервикальный канал — показана только глубокая конизация или ампутация шейки матки.
Выводы:
- Дисплазия шейки матки является предраковым процессом, с различным, в зависимости от степени тяжести, риском малигнизации.
- Дисплазия 1 (CIN 1, LSIL) в большинстве случаев проходит самостоятельно и зачастую не требует специального лечения.
- Дисплазия 2 и 3 (CIN 2-3, HSIL) связана с длительной персистенцией вируса папилломы человека в клетках, что приводит к их опухолевой трансформации.
- Дисплазия шейки матки диагностируется только с помощью цитологического исследования или гистологического исследования при биопсии.
- Положительный тест на онкогенные штаммы ВПЧ ни о чем не свидетельствует. Возможно, это транзиторная инфекция, которая у 90% женщин элиминируется в течение нескольких лет. Важность теста на ВПЧ повышается с возрастом.
- Использование презервативов и вакцинация являются наиболее эффективными и доказанными способами профилактики папилломавирусной инфекции.
Источник
Вирус папилломы человека -что это такое?
ВПЧ инфекция и аногенитальные бородавки.
Очень часто приходится сталкиваться с такой проблемой как ВПЧ- инфекция.
Обращаются молодые женщины с аногенитальными бородавками (остроконечными кондиломами) или с патологическими изменениями на шейке матки, вызванными влиянием ВПЧ- вирусом папилломы человека.
Это вызывает у женщин определенный страх, так как сегодня большинство женщин уже информированы о том, что вирус папилломы человека может вызывать развитие онкологических процессов и в частности рака шейки матки.
Поэтому хотелось бы дать немного информации о ВПЧ, устранить излишний страх, но в то же время насторожить, чтобы своевременно проходить скрининговое обследование.
И так, что же такое ВПЧ?
ВПЧ –это вирусы, принадлежащие к роду папилломавирусов. ВПЧ состоит 2-х цепочек ДНК, окруженных белками. ВПЧ — безкапсульный вирус, но он имеет капсид.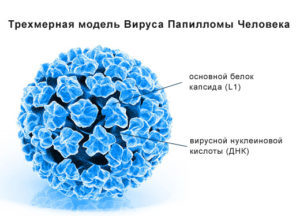
В настоящее время идентифицировано более 200 типов ВПЧ, 40 из них могут вызывать различные заболевания аногенитальной области.
ВПЧ поражает до 85% женщин в течении жизни!
Большинство женщин инфицируются с началом половой жизни и максимальная частота инфицированных достигается к 25 годам, а затем падает за счет самостоятельной элиминации, то есть ухода вируса из организма. Если элиминация не произошла, развиваются изменения шейки матки, ассоциированные с ВПЧ.
Пути передачи ВПЧ
- Половой путь (!) является наиболее частым путем передачи! ВПЧ относят к 6 -ой инфекции, передаваемой половым путем.
Половой путь:
 Генитально-генитальный
Генитально-генитальный
- Мануально-генитальный
- Орально-генитальный и др.
Неполовой путь (эстрагенитальный)
- Контакт с предметами/поверхностями, через которые можно возможна передача инфекции
- Вертикальная передача (от матери к новорожденному)
- Через кровь до рождения
- Во время прохождения через родовые пути
- Во время кесарева сечения с /без раннего повреждения оболочек
Все внеполовые пути передачи намного редки, по сравнению с половым путем!
ВПЧ проникает в клетки при тесном контакте эпителиальных тканей, к клеткам базального слоя эпидермиса. Вирус не располагается в поверхностных слоях эпителия, а проникает и инфицирует базальные клетки.
 ВПЧ обладает тропностью только к клеткам кожи и слизистых. ВПЧ проникает через поврежденный эпителий, в то время как здоровые эпителиальные клетки способны противостоять вирусу. Таким образом, лечение вагинальных инфекций и восстановление нормального биоценоза влагалища позволяет снизить онкологические риски!
ВПЧ обладает тропностью только к клеткам кожи и слизистых. ВПЧ проникает через поврежденный эпителий, в то время как здоровые эпителиальные клетки способны противостоять вирусу. Таким образом, лечение вагинальных инфекций и восстановление нормального биоценоза влагалища позволяет снизить онкологические риски!
Типы ВПЧ
В зависимости от типа, ВПЧ обладает высоким или низким онкогенным потенциалом, то есть способностью вызывать или не вызывать опухолевые процессы. ВПЧ низкоонкогенного типа как правило вызывают бородавки на коже, аногенитальные бородавки.
- Неонкогенные ВПЧ типы: 1−4,7,10, 28, 41 вызывают подошвенные, плоские и вульгарные бородавки.
- ВПЧ низкого онкогенного риска. Типы: 5−8, 11, 12, 14, 15, 17, 19−25, 42−44: аногенетальные кондиломы (АГК), ларенгиальный папилломатоз, бородавчатую эпидермоплазию.
Более 90% случаев аногенитальных бородавок обусловлены ВПЧ 6 и 11 типами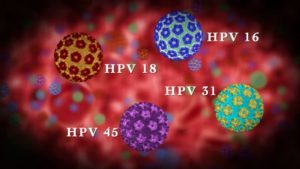
- ВПЧ высокого онкогенного риска 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68 могут вызывать раки самой различной локализации:
CIN I,II,III. (предраковое состояние)
Рак шейки матки
Рак прямой кишки
Рак влагалища и вульвы
Рак полового члена
Рак гортани
Рак ротовой полости
В 70% случаев РШМ (рак ш/матки) -вызывают 16-18 типы
В 70-90% случаев по разным данным ВПЧ может сам исчезнуть «уйти» без всяких вмешательств.
Простые типы ВПЧ «уходят», элиминируются в течение 6−12 месяцев.
Онкогенные типы –6−24 месяца.
Таким образом, молодые женщины с ВПЧ могут наблюдаться в течение 2-х лет, рассчитывая на самостоятельную элиминацию, но не более!!!
Из всех зараженных женщин вирусом папилломы человека, только у 7-10% процесс идет дальше переходя в CIN разной степени и рак, при определенных условиях!
Об этом надо помнить!
Стадии прогрессирования заболевания:
Проникая в клетку вирус долгое время может находится в организме в эписомальном состоянии, перстистируя, не проникая в ядро и не внедряется в геном клетки. Такое состояние называется вирусоносительство.
При бессимптомном носительстве и вирусовыделении: вирус спонтанно элиминирует в 90% случаев.
Постепенно базальные клетки проходят свой жизненный цикл: дифференцируются, поднимаются в поверхностные слои эпителия и слущиваются вместе с вирусом.
В этих случаях никаких изменений в клетках не происходит. Патологический процесс не развивается.
Латентная форма ВПЧ – это когда вирус выявляется в клетках эпителия, а морфологических изменений на шейке матки или в органах другой локализации нет.
Клиническая форма ВПЧ. При длительной персистенции вируса повышается риск внедрения ДНК вируса в геном базальных клеток — начинаются изменения, которые приводят к клиническим проявлениям в виде : CIN 1, CIN 2, CIN 3 или РШМ. Процесс может прогрессировать в течение 10−30 лет
В зависимости от степени поражения шейки матки вирусом различают предпатологическую стадию -CIN 1 — поражения низкой степени риска.
Спустя годы СIN 1 может прогрессировать до СIN 2 и CIN -3. Это уже поражение высокой степени риска и относится к предраковым состояниям.
CIN1 регрессирует самостоятельно в 60% случаев, персистирует — 30%, прогрессирует до CIN3 — 10%, прогрессирует до РШМ ( рак шейки матки)— менее 1%.

CIN2: регрессия — 40%, персистенция — 40%, прогрессирование — 20%, из них — 5% до инвазии.
CIN3: регрессия — 33%, персистенция — 55%, прогрессирование и инвазия — 12%.
Спустя десятилетия — рак.
Течение ВПЧ-инфекции зависит от активности иммунной системы. И может приводит либо к персистенции, либо кразвитию клинически значимых форм, либо к регрессу.
Диагностика ВПЧ инфекции
Кольпоскопическое исследование шейки матки необходимо проводить в 1 фазу цикла до 10-12 дня. Накануне исследования за 2-4 дня исключить половой контакт, свечи и другие манипуляции. Этот метод позволяет визуально увидеть поражения на ш/матки, характерные для ВПЧ инфекции и предположить вероятную степень поражения. Позволяет делать прицельные биопсии ш/матки
- ВПЧ-тестирование. ВПЧ тестирование – очень важный метод диагностики. Это определение ВПЧ методом ПЦР в материале, взятом из ц/канала. При ВПЧ — тестировании необходимо:
— Определять все онкогенные типы, а не только 16 и 18
— Обязательно определять вирусную нагрузку. Единицей измерения служит количественное содержание возбудителя на 100 000 клеток эпителия человека.
- Lg < 3 – концентрация ВПЧ клинически малозначимая и риск развития опухолевого процесса низкий.
- Lg 3-5 (на 10*5 эпителиальных клеток приходится геном-эквивалентов ВПЧ 10* 5 копий). Это клинически значимое количество ВПЧ, присутствует риск развития дисплазии;
- Lg > 5 (геномных эквивалентов ВПЧ 10 в 5 степени и более)
— Тест должен быть достоверным! Поэтому важно пользоваться надежными лабораториями!
- Молекулярные маркеры. В последние годы наибольшее внимание привлекают молекулярные маркеры пролиферации и озлокачествления p16INK4а и Е6/Е7 тРНК. Его применяют гистологи, когда не могут дифференцировать степень поражения.
- Биопсия. Это взятие ткани шейки матки на гистологическое исследование. Оно является последней инстанцией в постановке диагноза и определения степени поражения.
Возможны ошибки в постановке диагноза, если биопсия взята не в том месте! Например, рядом с пораженным участком. Поэтому желательно биопсию проводить под контролем кольпоскопа.
Тактика ведения при подозрении на CIN:
— Наблюдение?
— Лечение?
— Профилактика?
Выжидательная тактика
- У молодых женщин с CIN 1 , подтвержденном гистологически
- Жидкостная цитология проводится через 6 и 12 месяцев или альтернативно с ВПЧ –тестом через 12 месяцев.
- Интенсивное наблюдение необходимо в виду возможного риска нераспознанного поражения высокой степени в этой группе
Выжидательная тактика при CIN 1 сопряжена с риском, т.к. небольшой риск прогрессии сохраняется. И нет гарантии, что при биопсии не было пропущено CIN 2, 3
Выжидательная тактика при CIN 2,3 не допускается!
— За исключением беременных
— Молодых пациенток с CIN2 при небольшом поражении и удовлетворительной кольпоскопии.
Лечебная тактика при подозрении на ЦИН 2-3
Основной метод лечения это эксцизия или конизация ш/матки c обязательным гистологическим исследование. То есть удаление патологического участка на ш/матке с помощью радиоволн или лазерного луча.
Медикаментозного лечения ВПЧ в настоящее время нет, но разработки идут!
Препаратов, непосредственно влияющих на ВПЧ в мире нет!
Вирус может исчезнуть сам без какого либо лечения. Поэтому доказать эффективность препаратов, используемых для лечения ВПЧ очень трудно.
Все так называемые противовирусные препараты назначаются дополнительно к основному деструктивному лечению, с целью:
* Предупреждения прогрессирования заболевания.
* Устранения клинических проявлений заболевания.
* Уменьшения числа рецидивов.
Выбор препаратов иммунотропного действия для лечения вирусных инфекций
Существует ряд зарегистрированных препаратов, в показаниях к которым значится ВПЧ, однако, они не включены в рекомендации.
При применении лекарственных препаратов, воспроизводятся биологические эффекты эндогенных интерферонов, поэтому они являются средствами патогенетической терапии.
Наибольшее количество убедительных доказательных данных получено по 4 препаратам:
- изопринозин пранобекс
- ИФН
- глюкозаминилмурамилдипептид (ликопид)
- интерферон альфа-2b
В основе действия неспецифических иммуностимуляторов лежит активация клеток врожденного иммунитета и продукция эндогенных цитокинов, включая ИФН (интерферон) I и II типов, которые влияют на разные этапы жизненного цикла практически всех вирусов
Изопринозин пранобекс и глюкозаминилмурамилдипептид ( ГМДП) действуют системно, оказывая иммуностимулирующее и противовирусное действие + ГМДП обладает противовоспалительным эффектом, что очень важно, учитывая сочетание ВПЧ с другими инфекциями в 70−80% случаев. Оба препарата действуют за счет активации врожденного клеточного иммунитета.
Рекомендуемая продолжительность лечения: инозин пранобекс — 3−4 10-дневных курса с интервалом в 10−14 дней либо 28 дней; ГМДП — 1 курс 10 дней.
Наблюдение после лечения CIN 2,3
- ВПЧ тест или ВПЧ-тест + цитология через 6 месяцев после лечения.
- При отрицательном ВПЧ-тесте, необходимо ежегодное комбинированное тестирование – ВПЧ тест + жидкостная цитология.
- Позитивный ВПЧ-тест может обнаружить неудачу терапии рано и точно, даже при наличии нормальной цитологии, поэтому женщина продолжает интенсивно наблюдаться.
ВПЧ-тест — это стандарт постлечебной оценки!
Профилактика — вакцинация от ВПЧ
В 2008 году была присуждена Нобелевская премия за открытие роли ВПЧ в генезе рака шейки матки. В 99,7% случаев возникновения РШМ доказана роль ВПЧ! Рака шейки матки без ВПЧ насколько известно в настоящее время, не бывает!
На основе этого открытия были созданы профилактические вакцины:
- 2-х валентная- Церварикс — содержит инактивированные вирионы 16 и 18 типов
- 4- х валентная –Гардасил — содержит инактивированные вирионы 6, 11, 16 и 18 типов.
На сегодня существуют 9-валентная вакцина, но в РФ они не зарегистрированы.
В настоящее время уже прошло достаточно времени с момента начала применения вакцин, чтобы дать оценку эффективности вакцинации.
Австралийский анализ 2018г – у вакцинированных женщин от 18-35 лет наблюдается снижение аногенитальных бородавок и РШМ до 92%
Анализ Финляндии показывает практически 100% защиту от различных видов рака, ассоциированных с ВПЧ. Общая эффективность приравнивается к 100%
Вакцина показывает высокий профиль безопасности.
Вакцина безопасна! Редко могут быть покраснение, зуд в месте иньекции.
Исследования показывают, что иммунитет сохраняется и не требует повторной вакцинации.
На сегодняшний день время иммунного ответа от введения 4-х валентной вакцины пока не ограничивается.
86 стран включили вакцинацию девочек против ВПЧ в национальные календари прививок, 20 стран дополнили программы вакцинацией мальчиков
Вакцина является профилактической, а не лечебной! Поэтому самым лучшим и оптимальным вариантом является вакцинация до начала половой жизни, т.к с начала половой жизни большая вероятность заразиться ВПЧ
Вакцинацию оптимально делать с 9 до 12 лет. Можно вакцинировать двукратно, этого достаточно
На десять лет этой вакцины по наблюдениям хватает.
Вакцина к бесплодию не приводит. Это полная глупость, ерунда!
Сегодня вакцинировать можно до 45 лет!
Для вакцинации НЕТ необходимости определять наличие ВПЧ.
Сегодня определение ВПЧ делают с целью определения факторов риска и оценки излеченности после деструктивных методов лечения.
Если при скрининге ВПЧ нет, то можно следующее скрининговое исследование сделать через 3- 5 лет, т.к отсутствие ВПЧ не приведет к развитию онкологического процесса.
Наличие вируса – это всегда риск.! Но просчитать риск невозможно! Нужно наблюдение!
Вирус может как уйти из организма, так и начать неопластические процессы.
За ВПЧ онкогенного типа нужно наблюдать всю жизнь, если они не исчезнут.
Какая вакцина эффективнее?
И Церварикс, и Гардасил одинаково эффективны.
При использовании Церварикса титр антител выше, присутствует перекрестный эффект в отношении нескольких других типов.
У подростков и молодых женщин лучше использовать 4-х валентную вакцину Гардасил (лучше иммунный ответ и чаще встречаются генитальные кондиломы), а чем старше женщина, тем больше предпочтение — двухвалентной вакцине (более иммуногенна).
Имеет ли смысл вакцинировать уже инфицированных женщин?
Если речь идет о подростках и молодых женщинах — да, поскольку она на данный момент может быть инфицирована не онкогенным типом, а вакцина ее защитит в будущем от более опасного варианта инфекции или от рецидива ВПЧ-инфекции онкогенными типами.
Поговорим о РШМ.
РШ матки в РФ на первом месте в структуре смертности от злокачественных новообразований у женщин детородного возраста
В РФ в 2014 году этот показатель составил 20 человек на 100 000 (прирост на четверть по сравнению с 2004 годом).
Ежегодно в России регистрируется около 30 000 новых случаев ВПЧ – ассоциированных раков и более 1 000 000 случаев АБ (аногенитальных бородавок)
Показатели заболеваемости РШМ в РФ характеризуются тенденцией к росту и омоложению. Сегодня РШМ можно встретить у женщин в возрасте от 20 до 30 лет
Высокая доля запущенных случаев РШМ (3-4 ст — = 35%)
Высокий показатель смертности и одногодичной летальности (15,2%)
По данным ВОЗ в мире — более 270 000 женщин умирает ежегодно, но данные по разным странам сильно разнятся (в РФ — 8 человек на 100 000, прирост смертности за 10 лет — 7%).
Сегодня есть возможность полностью победить РШМ путем:
- массовой вакцинации девочек и мальчиков до начала половой жизни
- прохождения цервикального скрининга на РШМ — жидкостная цитология + ВПЧ тестирование с определением вирусной нагрузки
- повышения осведомленности населения об ИППП ( инфекций передающихся половым путем) — как фактор онкориска
- пропаганда Здорового образа жизни. ( отказ от курения и д,т)
Источник